Alessio Ruffini – matr. 117550 – Lezione del
9/10/2000 – ora 14.30 – 16.30
Esercizi 1° Principio della Termodinamica
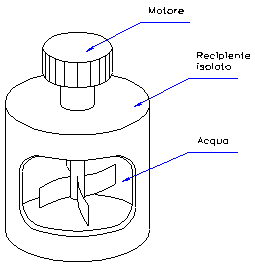
In questa lezione svolgeremo esercizi riguardanti il primo principio della termodinamica. In alcuni di questi utilizzeremo un recipiente (figura 1):
· termicamente isolato, cioè con Q = 0 (non si verifica scambio di calore con l’esterno e si trascurano i fenomeni al bordo del recipiente);
· che contenga, a seconda dell’esercizio, oggetti e sostanze diverse.
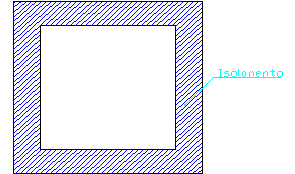
Figura 1
1º ESERCIZIO
Un recipiente termicamente isolato contiene 100 l d’acqua alla temperatura iniziale di 20°C. All’interno del recipiente vi è, inoltre, un’elica azionata da un motore della potenza di 0.5 CV, che dissipa energia meccanica per una durata t di 20 minuti (figura 2).
Determinare la variazione d’energia interna DU e la temperatura finale, sapendo che il recipiente è termicamente isolato: la trasformazione è a pressione costante e il calore specifico dell’acqua è pari a:
Cp
= 4187 ![]() (1)
(1)
Lezione del 9/10/2000 – ore 14.30–16.30
Figura 2
Nota:
In
quest’esercizio, come nei successivi, bisogna innanzi tutto accertarsi che
tutte le grandezze siano espresse nelle unità di misura del Sistema Internazionale, il SI contiene
le sette unità di misura fondamentali dalle quali si possono ricavare tutte le
altre ed è universalmente riconosciuto. Proprio per questo ci preoccuperemo di
tradurre tutte le grandezze che incontreremo in quelle riconosciute dal SI
(le tabelle di conversione sono inserite in fondo al capitolo).
Soluzione
I dati trasformati sono i seguenti:
L× = P = 0.5 × 736 = 368 W
M = 100 Kg
t = 20 × 60 = 1200 s
Utilizziamo ora il primo principio della termodinamica:
DU = Q
– L (2)
Dato che, per ipotesi, non avviene scambio di calore con l’esterno (Q = 0) e che è un lavoro fatto su sistema (quindi negativo), la formula semplificata è la seguente:
DU = - ( - P× t ) = 368 × 1200 = 441600 J (3)
Lezione del 9/10/2000 – ore
14.30–16.30
Posso calcolare la DU specifica (rispetto alla massa, cioè la variazione per unità di massa):
Du = ![]() =
= ![]() = 4416 ×
= 4416 × ![]() (4)
(4)
Utilizzando la formula che lega il calore specifico Cp alle temperature, quella finale TF e quell’iniziale TI, ottengo il risultato finale:
4416![]() = Cp (TF - TI) (5)
= Cp (TF - TI) (5)
quindi:
TF = TI + ![]() = 293 +
= 293 + ![]() = 294,05 K
= 294,05 K
2º ESERCIZIO
Un recipiente termicamente isolato contiene 100 l d’acqua alla temperatura iniziale di 20°C.
All’interno del recipiente vi è, inoltre, un albero azionato da una puleggia aggravata da un peso di 100 Kg che, tramite un’elica, dissipa energia meccanica.
Nel recipiente vi è anche una resistenza di 0.2 W che dissipa calore per effetto Joule. Attraverso questa resistenza circola una corrente di 6 A, per un periodo t di 5 minuti (figura 3).
L’effetto dell’energia elettrica deve equivalere a quello dell’energia meccanica prodotta dalla caduta del grave. In base a ciò determinare il dislivello DZ da cui deve cadere il grave.
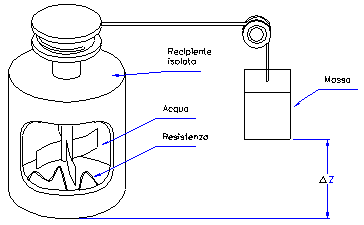
Figura 3
Lezione del 9/10/2000 – ore
14.30–16.30
Soluzione
I dati trasformati sono i seguenti:
M = 100Kg
t = 5 × 60 = 300 s
Utilizzando il primo principio ricaviamo:
DU = Q = R × i 2 × t = 0,2 × 6 2 × 300 = 2160 J (6)
Abbiamo ottenuto questo risultato perché la variazione d’energia, dovuta alla resistenza, è data dal solo contributo del calore.
La variazione d’energia DU dovuta alla massa che cade è:
DU = - L = + M × g × DZ (7)
quindi:
DZ = ![]() = 2.20 m
= 2.20 m
Il lavoro è negativo, perché svolto su sistema, inoltre non c’è scambio di calore siccome stiamo verificando il primo principio sull’universo e non all’interno del sistema.
3º ESERCIZIO
Una massa di gas compie una trasformazione da uno stato iniziale A ad uno stato finale B attraverso diversi stati fisici.
L’espansione da A a B può avvenire attraverso 3 differenti percorsi (figura 4):
a) la curva blu nel grafico rappresenta una trasformazione isobara (pressione costante) seguita da un’isocora (volume costante);
b) la linea rossa rappresenta una trasformazione in cui la pressione ed il volume
variano linearmente;
c) la curva verde rappresenta una trasformazione adiabatica, vale a dire una trasformazione lungo la quale in nessun punto vi è scambio di calore, quindi Q = 0 non solo nel punto iniziale e finale ma lungo tutti i punti della trasformazione.
La nostra trasformazione adiabatica è del tipo:
p× v![]() =
cost. (8)
=
cost. (8)
Lezione del 9/10/2000 – ore
14.30–16.30
Determinare il lavoro nelle tre trasformazioni.
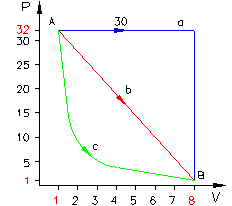
Figura 4
Nota:
In alcuni casi particolari si può seguire la
trasformazione punto per punto (detta trasformazione “quasi statica”). Essa
procede per punti contigui uniformemente vicini.
Esempio:
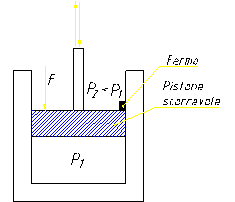
Figura 5
Quando il fermo viene
tolto (figura 5) si ha un’espansione del gas seguita da una compressione
poiché P2 < P1. Questo fenomeno continua con
intensità sempre minore fino a che le due pressioni si equivalgono; ciò si può
paragonare allo smorzamento di una molla (figura 6).
Lezione del 9/10/2000 – ore 14.30–16.30
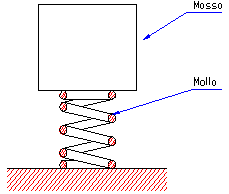
Figura
6a
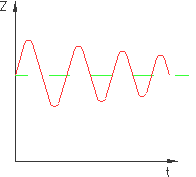
Figura 6b
Una trasformazione di questo tipo non è quasi statica,
quindi occorre una forza F che privi il pistone di brusche accelerazioni
(rendendo le variazioni infinitesime).
Ciò è importante poiché, se la trasformazione non è quasi statica, si disegnano diagrammi relativi errati quindi occorre sempre lavorare con trasformazioni quasi statiche.
Soluzione
I dati trasformati sono i seguenti:
VA
= 0,001 m3 ,
VB = 0,008 m3
PA = 32 × 105 Pa ,PB = 1ּ105
Pa
Calcoliamo il lavoro lungo la trasformazione c (figura 7a) :
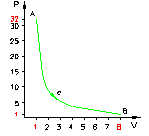
Figura 7a
Lezione del 9/10/2000 – ore 14.30–16.30
in questa trasformazione non vi è scambio di calore quindi il 1° principio diventa:
![]() (9)
(9)
Sapendo inoltre che il lavoro è uguale all’area sottesa dalla curva c otterremo:
![]() (10)
(10)
la formula (10) è stata ricavata, utilizzando le grandezze intensive, mentre senza si ha:
![]() (11)
(11)
Sfruttando i dati iniziali ricaviamo:
![]() (12)
(12)
quindi :
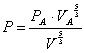
allora, risolvendo l’integrale otteniamo:
L 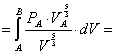 (13)
(13)
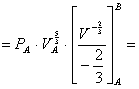
![]()
![]()
![]()
introducendo in valori numerici l’equazione diviene:
![]()
Lezione del 9/10/2000 – ore 14.30–16.30
Ora esaminiamo il cammino lungo la curva a (figura 7b): il lavoro è semplicemente l’area sottesa dalla curva blu.
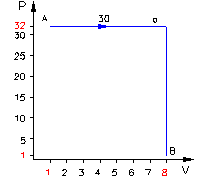
Figura 7b
![]() (14)
(14)
Notiamo che il lavoro lungo a è più grande mentre l’energia interna è la stessa.
Sapendo che ![]() otteniamo:
otteniamo:
![]() (15)
(15)
Quindi la trasformazione a è migliore della c, poiché il calore ricevuto dall’esterno è stato trasformato in lavoro e quindi si può sfruttare.
Esaminiamo ora il cammino lungo la linea rossa b
(figura 7c):
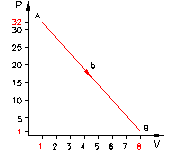
Figura 7c
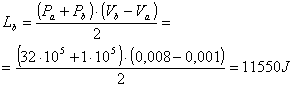 (16)
(16)
Lezione del 9/10/2000 – ore
14.30–16.30
Analogamente a prima otteniamo:
![]()
Quindi si è prodotto meno lavoro poiché si è ricevuto meno calore dall’esterno.

Figura 8
Soluzione
I dati
trasformati sono ![]() e
e ![]() (pressione iniziale).
(pressione iniziale).
Sfruttando la legge dei gas perfetti, abbiamo quest’ equazione:
![]() (17)
(17)
La temperatura T si mantiene costante durante la trasformazione perciò l’equazione diventa questa:
![]() (18)
(18)
Lezione del
9/10/2000 – ore 14.30–16.30
quindi:
![]() (18)
(18)
Il lavoro è invece rappresentato dall’area tratteggiata in blu e in rosso, quindi:
![]() (19)
(19)
Osserviamo che questa equazione è corretta nella logica del sistema, però ciò non rappresenta il lavoro effettivamente svolto dalla persona che spinge il pistone, infatti anche la pressione ambientale svolge un lavoro e precisamente l’area tratteggiata in rosso quindi:
![]() (20)
(20)
Consideriamo che il nostro sistema non sia solo isolato, ma addirittura raffreddato in modo tale da mantenere la temperatura costante quindi possiamo scrivere:
![]() (21)
(21)
continuando:
![]() (22)
(22)
quindi risolvendo e inserendo i valori numeri otteniamo:
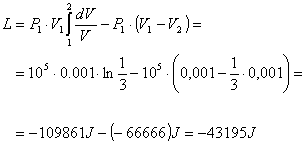
Il lavoro è negativo perché è ricevuto dal sistema.
Lezione del 9/10/2000 – ore 14.30–16.30
Siamo così arrivati alla pressione P2.
A questo punto, scatta la valvola della camera ad aria (figura 9) e il sistema da chiuso diventa aperto. Esce l’aria rimanente dalla pompa fino a quando il pistone arriva a fine corsa.
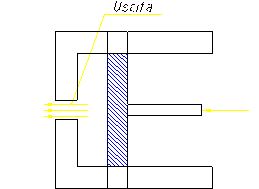
Figura 9
A questo
punto, si ritorna indietro.Entra l’aria attraverso la guarnizione alla
pressione di 1 atm. Osservando la figura 10, m’accorgo che ![]() ma è l’energia
interna del sistema chiuso. Se considero anche l’aria che entra nella pompa, ho
un
ma è l’energia
interna del sistema chiuso. Se considero anche l’aria che entra nella pompa, ho
un
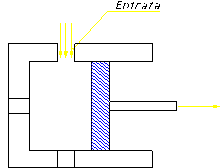
Figura 10
sistema
aperto e quindi non vale più la reazione precedente che si rifaceva al 1º PRINCIPIO
della TERMODINAMICA
Durante la compressione, ho ricevuto lavoro dall’ambiente mentre ne ho ceduto all’ambiente durante l’espansione del pistone: i due lavori risultano coincidenti e sono uguali a (figura 11):
![]() (23)
(23)
Lezione del 9/10/2000 – ore
14.30–16.30
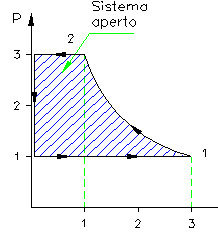
Figura 11
Osserviamo che non è importante quale sistema di riferimento sia stato preso, purché alla fine, il lavoro coincida in ogni sistema.
NOTA:
Questi ultimi tre esercizi si possono risolvere intuitivamente, però cercheremo di spiegarli in modo più rigoroso.
5º ESERCIZIO
Una pompa
preleva dell’acqua da una fontana. Alla sommità della pompa si registra, con un
barometro, la pressione di ![]() .
.
Calcolare la prevalenza della pompa, cioè l’altezza teorica Z a cui la pompa potrebbe sollevare l’acqua (figura 12).
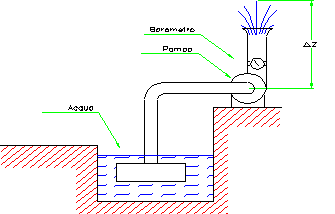
Figura 12
Lezione del 9/10/2000 – ore
14.30–16.30
Soluzione:
Dalle tabelle in fondo al capitolo apprendiamo che la pressione atmosferica è equivalente ad una colonna di mercurio alta 760 mm.
Poiché vale,ovviamente la seguente relazione:
![]() (24)
(24)
Ne consegue che:
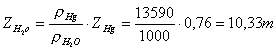 (25)
(25)
quindi la prevalenza vale:
![]()
6º ESERCIZIO
Un uomo si
trova 20 m sott’acqua e riceve aria da una bombola che eroga ossigeno
alla stessa pressione in cui si trova, cioè a 200 bar (figura 13).
L’uomo prende una boccata d’aria e, supponendo che abbia nei polmoni 6 l di ossigeno, determina a quanto equivale la forza di galleggiamento.
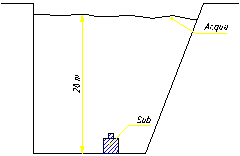
Figura 13
Soluzione:
L’uomo riceve aria dalle bombole alla pressione di 3 bar (1 bar dovuto all’atmosfera, 2 per la profondità di 20 m).
L’aria, una volta entrata nei polmoni, forma con questi un sistema termodinamico chiuso a temperatura costante (quella del corpo umano).
Lezione del
9/10/2000 – ore 14.30–16.30
Quindi dalla legge dei gas abbiamo che:
![]() (26)
(26)
Una volta in superficie, la pressione è quella atmosferica di 1 bar quindi il volume V2 sarà:
![]() (27)
(27)
L’uomo galleggia poiché il suo volume è aumentato di 12 l e il suo peso è rimasto invariato.
All’inizio l’uomo si trovava sotto il livello dell’acqua di 20 m. Ora, grazie ai 12 l di volume in più, avrà una forza di galleggiamento pari a:
![]() (25)
(25)
7º ESERCIZIO
Una pentola contiene 10 libbre d’acqua e viene scaldata con una fiamma che fa passare la temperatura da 0º R a 80º R e da 32º F a 212º F (figura 14).
Qual è la quantità di calore Q necessaria affinché ciò avvenga?
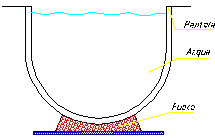
Figura 14
Soluzione:
I dati trasformati sono i seguenti:
10 libbre = 4356 g
0º R = 0º C
80º R = 100º C
0º F = 0º C
212º F = 100º C
In entrambi i casi, la quantità di calore necessaria sarà la stessa.
Dalla definizione di caloria si ricava che per aumentare di 100º C 1 g d’acqua occorrono 100 calorie. Quindi la quantità di calore necessaria nel nostro caso è:
![]()
Lezione del 9/10/2000 – ore 14.30–16.30
TABELLE
Pressione
|
Pa |
atm |
bar |
torr (mmHg) |
mH2O |
kp/cm2 |
|
Pa |
1 |
9.87×10-6 |
10-5 |
7.5×10-3 |
1.019×10-4 |
1.019×10-5 |
|
atm |
1.013×105 |
1 |
1.013 |
760 |
10.33 |
1.033 |
|
bar |
105 |
0.9869 |
1 |
750 |
10.2 |
1.02 |
|
torr (mmHg) |
1.333×102 |
1.31×10-3 |
1.33×10-3 |
1 |
0.0135 |
0.00135 |
|
mH2O |
9.81×103 |
0.0968 |
0.098 |
74 |
1 |
0.1 |
|
kp/cm2 |
9.81×104 |
0.968 |
0.98 |
740 |
10 |
1 |
Legenda:
Pa = Pascal
Torr = torricelli o mm di mercurio
mH2O = metri di acqua
kp/cm2 = chilogrammo su centimetroquadrato
Potenza
|
W |
HP |
Kpm/s |
Kcal/h |
|
|
W |
1 |
1,36×10-3 |
1,34×10-3 |
0,102 |
0,8598 |
|
CV |
736 |
1 |
0,986 |
75 |
632,81 |
|
HP |
745,2 |
1,014 |
1 |
76,04 |
640,72 |
|
Kpm/s |
918 |
0,01333 |
0,01315 |
1 |
8,426 |
|
Kcal/h |
1,163 |
1,581×10-3 |
1,558×10-3 |
0,118 |
1 |
Legenda:
W = watt
Kpm/s = kilogrammetro al secondo
Kcal/h = chilocaloria su ora
Energia
|
J |
CVh |
erg |
cal |
eV |
BTU |
Kgm |
|
J |
1 |
3,77×10-7 |
107 |
0,239 |
6,24×1018 |
9,47×10-4 |
0,1 |
|
CVh |
2,65×106 |
1 |
2,65×1013 |
0,63×106 |
16,5×1024 |
2,5×103 |
2,65×105 |
|
erg |
10-7 |
3,77×10-14 |
1 |
0,239×10-7 |
6,24×1011 |
9,47×10-11 |
0,1×10-7 |
|
cal |
4,184 |
15,77×10-7 |
4,184×107 |
1 |
26,1×1018 |
39,6×10-45 |
0,418 |
|
eV |
1,602×10-19 |
6×10-26 |
1,602×10-12 |
3,82×10-20 |
1 |
15,15×10-23 |
1,602×10-20 |
|
BTU |
1055 |
3,97×10-4 |
10,55×109 |
252 |
6,58×1021 |
1 |
105,5 |
|
Kgm |
9.807 |
3,7×106 |
9.807×10-7 |
2,34 |
6,1×1019 |
9,2810-3 |
1 |
Lezione del 9/10/2000 – ore
14.30–16.30
Legenda:
J = Joule
cal = caloria
eV = elettronvolt
BTU = British termal unit
Kgm = Kilogrammetro
Densità
|
|
|
acqua |
1000 |
|
mercurio |
13590 |
|
Acqua del mare |
1025 |
|
Freon 12 |
1327 |
|
benzene |
881 |
|
metanolo |
791 |
Temperatura
|
Congelamento dell’acqua |
Ebollizione dell’acqua |
|
K Kelvin |
273,15 |
373,15 |
|
ºC Celsius |
0 |
100 |
|
ºF Fahrenheit |
32 |
212 |
|
ºR Réamur |
0 |
80 |
Relazione fra scale di
temperatura:
T(K) = T(˚C)
+ 273,15 = 5/9 T(ºF) + 255,37
= 5/4 T(ºR) +
273,15
T(˚C) =
T(K) – 273,15 = 5/9 [T(ºF) –
32] = 5/4 T(ºR)
T(ºF) = 9/5 [T(K) – 255,37] = 9/5 T(˚C) + 32 = 9/4 T(ºR) + 32
T(ºR) = 4/5 [T(K) – 273,15] = 4/5 T(˚C) = 4/9 [T(ºF) – 32 ]
Relazione fra scale di peso:
1 lb(GB) = 453.6 ּ 10-3
1 lb(USA) = 435,6 ּ 10-3