Il secondo principio della termodinamica
Il rendimento di conversione
Il primo principio della
termodinamica stabilisce che l’energia non si crea e non si distrugge, può
essere trasformata nella forma ma l’energia totale rimane invariata. Tuttavia
possiamo pensare a numerosi processi termodinamici che in realtà non possono
avvenire pur non violando il primo principio. Per esempio quando un corpo
freddo ed uno caldo vengono a contatto, non può accadere che il corpo caldo si
scaldi e quello freddo si raffreddi, anche se in essi l’energia si conserva..
Allo stesso modo, tale principio non pone alcuna restrizione alla possibilità
di convertire lavoro in calore o calore in lavoro. In pratica, però, non è MAI
possibile convertire COMPLETAMENTE una data quantità di calore in lavoro. Il
secondo principio della termodinamica specifica perciò quali processi, ,
avvengono in natura e non violano il primo principio.
Dal primo principio si
può dedurre che le forme di energia sono tutte uguali. In realtà questo è vero
solo dal punto di vista quantitativo ma non qualitativo, infatti l’energia può
essere più o meno pregiata a seconda del suo rendimento al momento della
conversione. Questo richiede di definire il concetto di RENDIMENTO DI
CONVERSIONE(![]() ):
):
![]()
(1)
dove
l’![]() <
< ![]() perché in un processo
di conversione, dell’
perché in un processo
di conversione, dell’![]() che facciamo entrare nel “convertitore”, una parte viene
convertita, ed una parte viene
dissipata nell’ambiente o rimane intrappolata all’interno del sistema.
che facciamo entrare nel “convertitore”, una parte viene
convertita, ed una parte viene
dissipata nell’ambiente o rimane intrappolata all’interno del sistema.
![]()
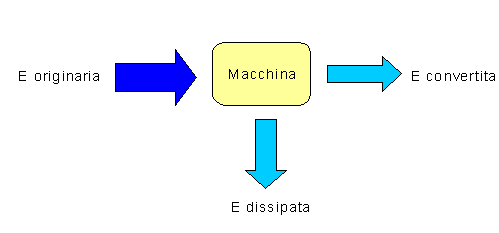
![]() Fig.1 Sistema di conversione
Fig.1 Sistema di conversione
Per
il primo principio deve essere
ovviamente
![]() =
= ![]() +
+ ![]()
(2)
Se prendiamo ad esempio una batteria,
nel convertire energia elettrica in energia chimica, libera calore ( ![]() ) che normalmente non ha valore o addirittura è un danno;
pertanto si vorrebbe realizzare un sistema di conversione in grado di
convertire integralmente tutta l’energia da qualunque forma a qualunque altra
senza alcuna dispersione.
) che normalmente non ha valore o addirittura è un danno;
pertanto si vorrebbe realizzare un sistema di conversione in grado di
convertire integralmente tutta l’energia da qualunque forma a qualunque altra
senza alcuna dispersione.
Possiamo dire di avere diverse categorie di energia. Se consideriamo l’energia elettrica, ad esempio, questa è altamente convertibile e viene definita NOBILE, poiché da essa possiamo ricavare facilmente tutte le altre forme di energia con un rendimento del 100%. La problematica diventa più complessa quando partiamo da un’energia meno nobile come il calore (Q) poiché la sua convertibilità è estremamente più bassa e in ogni caso si ha un limite massimo del rendimento di conversione << 1. In particolare il 30% di energia viene convertita ed è detta EXERGIA, il 70% dissipata ed è detta ANERGIA.
Pertanto data una quota
complessiva di energia essa si scompone sempre in una frazione anergetica ed in
una exergetica, ed è proprio da quest’ultima che dipende il valore dell’energia
stessa.
Enunciazione del secondo principio della termodinamica
Il secondo principio della termodinamica stabilisce il valore di convertibilità massimo dell’energia termica nelle altre forme di energia in funzione della temperatura. L’enunciato afferma che l’energia termica non è convertibile in lavoro con un rendimento prossimo a 1, ossia è impossibile ottenere solo lavoro dal calore. Questo può anche essere espresso tramite un paradosso che è il cosiddetto MOTO PERPETUO. Esistono tre specie di tale moto:
1° Specie : è il moto perpetuo di un sistema che senza nessun apporto energetico
dall’esterno produce lavoro. Ossia l’energia dovrebbe scaturire dal nulla e ciò
violerebbe il primo principio. Tale moto non può dunque esistere.
2° Specie : è una macchina, costituita da un sistema al quale noi forniamo
calore, che produce una quantità di
lavoro che in Joule pareggia perfettamente il calore fornito. L’energia
dissipata dovrebbe essere nulla, ma questo andrebbe contro il secondo
principio. Nemmeno questo moto può esistere, a meno che l’energia fornita non
sia integralmente convertibile (es. energia elettrica).
3° Specie : è un sistema privo di attrito in cui si produce moto senza lavoro. Il
moto perpetuo di terza specie esiste ( es. la Terra ) ed è realizzabile a patto che si rinunci a sottrargli lavoro,
poiché in tal caso in breve tempo il moto cesserebbe. Questo concetto fu stabilito
già nel Diciassettesimo secolo da Newton con la formulazione del principio
d’inerzia secondo cui un corpo persevera nel suo stato di quiete o di moto
rettilineo uniforme finché non agiscono forze che ne modifichino lo stato.
Seconda forma dell’enunciato del secondo principio della termodinamica
Il secondo principio della termodinamica viene
espresso in due differenti forme: la
prima, che abbiamo già visto, fu enunciata da Kelvin e nega il moto perpetuo di
seconda specie, quindi la possibilità di ottenere come unico risultato la conversione
integrale di calore in lavoro; la seconda invece, enunciata da Clausius, nega
la possibilità di avere una macchina frigorifera che lavora senza bisogno di
lavoro esterno.
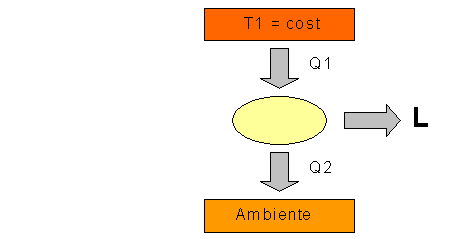
Fig. 2 Sistema
diretto
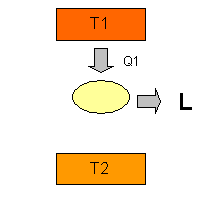
Se da un serbatoio, una
sorgente di calore a temperatura costante ![]() , si estrae il calore
, si estrae il calore ![]() per fornirlo ad una
macchina che deve fare il processo di conversione, questa produrrà un lavoro L;
ma poiché il secondo principio della termodinamica dice che ciò non può
essere l’unico risultato, la macchina produrrà anche un calore
per fornirlo ad una
macchina che deve fare il processo di conversione, questa produrrà un lavoro L;
ma poiché il secondo principio della termodinamica dice che ciò non può
essere l’unico risultato, la macchina produrrà anche un calore ![]() che verrà ceduto
all’ambiente.
che verrà ceduto
all’ambiente.
Supponiamo ora che tutto avvenga con
macchine perfettamente reversibili e che tutte le frecce si invertano:
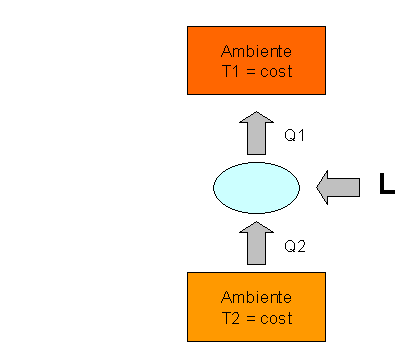
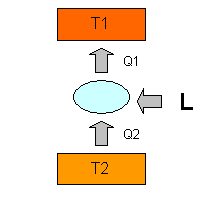
Fig. 3 Sistema inverso: macchina frigorifera
In
questo caso la macchina invece che erogare lavoro lo assorbe: prende il calore ![]() da un ambiente a temperatura
da un ambiente a temperatura ![]() e lo pompa ad un
altro ambiente a temperatura
e lo pompa ad un
altro ambiente a temperatura ![]() .
.
Questa
è quella che chiamiamo macchina frigorifera, che anziché prendere del calore e
produrre lavoro stabilisce un flusso di calore tra due ambienti a temperatura
diversa. In particolare, considerando ![]() <
<![]() , la macchina prende calore da un ambiente freddo e trasporta
questa energia in un ambiente più caldo, contrariamente a quanto avviene in
natura.
, la macchina prende calore da un ambiente freddo e trasporta
questa energia in un ambiente più caldo, contrariamente a quanto avviene in
natura.
|
|
PROIBITE |
PERMESSE |
|
K E L V I N |
|
|
|
CL A U S I U S |
|
|
Fig. 4 Trasformazioni permesse e
proibite in base agli enunciati di Kelvin e Clausius
La formula di Carnot
A questo punto si tratta di dare all’enunciato del secondo principio della termodinamica una formulazione numerica. Tale formulazione viene associata a Carnot, il quale, nella prima metà dell’ottocento ( 50 anni prima dell’enunciazione del secondo principio ) ebbe modo di utilizzare e progettare macchine a vapore in grado di convertire il calore in lavoro.
Fu proprio studiando la progettazione
di queste macchine che Carnot si rese conto che qualunque cosa si facesse per
migliorarle, esse hanno sempre un limite massimo di conversione oltre al quale
non si poteva andare. Tale limite venne formalizzato in una formula detta
appunto formula di Carnot. Carnot definì il rendimento di conversione con una
terminologia diversa da quella che abbiamo esaminato precedentemente (![]() ), infatti egli
definì un altro numero detto COEFFICIENTE ECONOMICO DELLA MACCHINA A VAPORE
), infatti egli
definì un altro numero detto COEFFICIENTE ECONOMICO DELLA MACCHINA A VAPORE
![]()
(3)
E’ evidente che anche questo
coefficiente , come il ![]() , è definito dal rapporto
tra l’energia convertita L e il calore da convertire
, è definito dal rapporto
tra l’energia convertita L e il calore da convertire ![]() , rapporto che può
andare a 1 se tutto il calore venisse convertito in lavoro. Ma poiché esiste un
calore
, rapporto che può
andare a 1 se tutto il calore venisse convertito in lavoro. Ma poiché esiste un
calore ![]() non trascurabile, l’espressine ricavata ha un
risultato limitante che indica esattamente il massimo grado di conversione di
calore in lavoro ( Fig. 2 ).
non trascurabile, l’espressine ricavata ha un
risultato limitante che indica esattamente il massimo grado di conversione di
calore in lavoro ( Fig. 2 ).
Il coefficiente economico di Carnot, a
suo tempo, era stato definito per le macchine a vapore, ma è concettualmente
estendibile a una qualunque macchina che operi tra due serbatoi a temperatura
costante dove, per serbatoio, intendiamo un particolare sistema la cui
temperatura non cambia anche aggiungendo o sottraendo calore ( es. acqua che
bolle o contenitore con acqua e ghiaccio ).
Il ciclo di Carnot
Supponiamo che la macchina prima rappresentata sia
una macchina ciclica ossia una macchina che una volta terminato il ciclo torna
esattamente allo stato fisico iniziale. Poiché l’energia è una funzione di
stato, l’energia intrappolata dentro la macchina non cambia, o meglio cambia
durante il ciclo ma alla fine di esso torna al punto di partenza. Quindi se
considero un numero intero di cicli posso di fatto fare un bilancio
dell’energia tra ![]() e L trascurando la variazione di
energia durante il ciclo. Ricavo che
e L trascurando la variazione di
energia durante il ciclo. Ricavo che
![]()
(4)
e quindi
![]()
(5)
Questo é vero per qualsiasi macchina; ma Carnot volle fare una macchina migliore di tutte le altre ossia quella con il massimo coefficiente economico e ottenne
![]() .
.
(6)
Il rapporto tra le temperature
scambiate è esattamente uguale al rapporto tra le temperature dei due serbatoi
(![]() ).
).
Questa è l’espressione come formula del
secondo principio della termodinamica perchè stabilisce esattamente quale è la
frazione di energia convertibile in lavoro. E’ evidente analizzando le formule
che per avere un maggior grado di convertibilità del calore in lavoro devo far
crescere la ![]() e far calare la
e far calare la ![]() .
.
Macchine frigorifere e pompe di calore
Il teorema
di Carnot è stato enunciato per i sistemi diretti cioè quelli che producono
lavoro a spese di calore ma esistono anche macchine inverse ( frigorifere ) che
prendono lavoro dall’esterno e trasportano calore dal serbatoio freddo a quello
caldo. In questo caso non si usa più il coefficiente economico così definito ![]() , ma si definisce un nuovo tipo di rendimento che è
concettualmente sempre il rapporto tra ciò che ho ottenuto e ciò che ho speso
ma questa volta ho ottenuto due cose: del freddo perché ho sottratto calore ad
un ambiente e del caldo perché ho fornito calore ad un altro. D’estate cercherò
di sfruttare il freddo che la macchina produce e quindi definiremo un
rendimento estivo
, ma si definisce un nuovo tipo di rendimento che è
concettualmente sempre il rapporto tra ciò che ho ottenuto e ciò che ho speso
ma questa volta ho ottenuto due cose: del freddo perché ho sottratto calore ad
un ambiente e del caldo perché ho fornito calore ad un altro. D’estate cercherò
di sfruttare il freddo che la macchina produce e quindi definiremo un
rendimento estivo
![]()
(7)
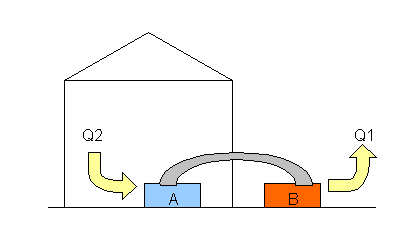
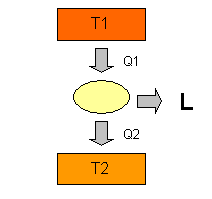
Fig. 5 Il condizionatore
D’estate B diventa caldo ed espelle il
calore Q1 mentre A si raffredda e prende il calore Q2.
D’inverno cercherò invece di sfruttarne il caldo, definendo anche un rendimento invernale
![]()
(8)
La macchina utilizzata in questo modo viene definita POMPA DI CALORE.
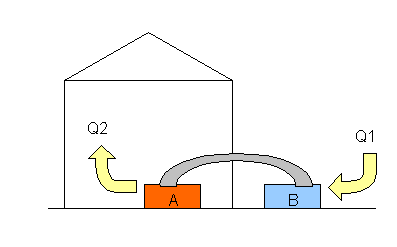
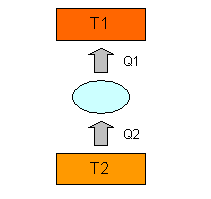
Fig. 6 Pompa di calore
Questa volta, in inverno, A produce calore e scalda la stanza, mentre B si raffredda.
Se consideriamo che il nostro
condizionatore sia davvero una macchina di Carnot allora ![]() e possiamo definire una relazione tra
e possiamo definire una relazione tra ![]() e
e ![]() .
.
![]()
(9)
In pratica il ![]() è sempre migliore del
è sempre migliore del
![]() .
.
La situazione
energetico ambientale del Paese
La macchina frigorifera, nonostante i suoi enormi vantaggi viene comunemente utilizzata solo come impianto di condizionamento estivo. Solamente negli edifici pubblici vengono sfruttate a pieno le sue potenzialità in quanto il riscaldamento ad aria canalizzata garantisce il ricambio dell’aria, evita la produzione di prodotti della combustione e riduce al minimo quelli che possono essere i rischi di un impianto a gas.Tali macchine però comportano costi iniziali abbastanza elevati che grazie però al loro minor consumo energetico porteranno ad un risparmio a lungo termine.
Lo scarso utilizzo di tali macchine è dovuto ad una politica energetica errata i quanto in Italia si è preferito incentivare i consumi del combustibile primario ( come il gas ) in forma diretta che dimostrano una mancata comprensione del secondo principio che porterebbe invece ad assegnare all’energia un valore differenziato.
Un caso particolare è rappresentato dalla provincia di Brescia.Qui è stata realizzata una grande centrale che produce e vende direttamente ai cittadini sia acqua calda che energia elettrica, in questo modo i problemi di inquinamento e sicurezza sono notevolmente diminuiti. In termini economici l’azienda municipalizzata di Brescia è una delle più ricche di Italia perché è riuscita in un certo qual modo a vendere due volte lo stesso prodotto. Infatti, poiché l’energia elettrica viene normalmente venduta ad un prezzo che corrisponde al costo industriale di trasformazione di questa intera quantità di calore in una parziale quantità di lavoro, tutto quello che ne esce sotto forma di energia dissipata ( acqua calda ) viene a sua volta fatta pagare.
La centrale si preoccupa di fornire acqua calda a coloro che risiedono nelle zone limitrofe ad essa, mentre fornisce energia elettrica, più facilmente trasportabile, alle abitazioni più distanti per poi essere riconvertita in calore a destinazione con tariffe equivalenti.
Consumi energetici
nazionali nei vari settori
InItalia i consumi di energia continuano a crescere in modo disuguale a seconda che si considerino gli utilizzi domestici, quelli industriali e i trasporti. I consumi di energia dell’industria nel 1997 incidono per circa un terzo del fabbisogno energetico nazionale. C’è stato negli ultimi anni un consistente aumento di efficienza nell’impiego dell’energia accompagnato ad un significativo ridimensionamento nell’utilizzo diretto dei prodotti petroliferi, infatti, questi rappresentavano il 58% dei consumi dell’industria nel 1971 ma oggi coprono meno del 18%. Si è registrata contemporaneamente una massiccia crescita nell’impiego di gas naturale che si colloca oggi al primo posto con una quota pari al 40% del fabbisogno.
Diverse sono invece le considerazioni che investono gli utilizzi civili dell’energia. Nel 1998 i consumi sono stati pari al 29,5% dei consumi nazionali, con una larga predominanza del gas naturale che copre più della metà della richiesta complessiva, per un quarto soddisfatta dall’energia elettrica e per il restante 20% dai derivati petroliferi e dalla legna con un apporto trascurabile del carbon fossile. Nel ultimo quindicennio si è registrato un rapido calo nell’impiego di prodotti petroliferi con l’impennata dei consumi di gas naturale e con una costante crescita della richiesta di energia elettrica. Nell’ambito degli impieghi civili la quota più consistente dei prelievi di energia è rappresentata dal riscaldamento, dove il gas copre una quota pari al 68,8% grazie anche alla forte diffusione dei sistemi autonomi.
In crescita anche i consumi di energia elettrica ripartiti tra settore residenziale (56,9%) e settore terziario (43,1%). L’aumento della domanda è nettamente più rilevante per gli impieghi terziari cresciuti, negli ultimi otto anni del 40%, rispetto ad una crescita del 12% nel settore abitativo. L’85% della domanda di elettricità per impieghi civili riguarda un numero limitato di apparecchiature che nell’ordine sono: scaldacqua, frigoriferi, lampade, lavatrici, televisori, lavastoviglie e cucine miste.
È in particolare nel settore dei trasporti che si concentrano le maggiori preoccupazioni degli esperti. Tra il 1975 e il 1995 i consumi imputabili all’attività di trasporto sono di fatto raddoppiati passando da 18,9 a 37,8 milioni di tonnellate. Il 90% di questi consumi è imputabile al trasporto stradale in particolare il 75% è dovuto alla mobilità delle persone, il restante 25% alla mobilità delle merci. L’Italia risulta così essere nell’ambito dei paesi Ocse quello con la più alta percentuale di traffico stradale passeggeri per unità di prodotto interno lordo e per abitante. Desta preoccupazione il forte impatto ambientale dovuto a questo fenomeno. Infatti i trasporti stradali contribuiscono per il 24% alle emissione di anidride carbonica, per il 73% a quelle di monossido di carbonio, per il 52% a quelle di ossido di azoto, e per il 52% a quelle di idrocarburi volatili non metanici.
L’insieme dei fenomeni descritti si è tradotto a livello di Sistema Paese, in un sensibile cambiamento della copertura del fabbisogno energetico nazionale. Nel corso dell’ultimo decennio il gas naturale è stata la fonte che ha registrato il tasso di crescita più elevato più del 4,4% in media all’anno.
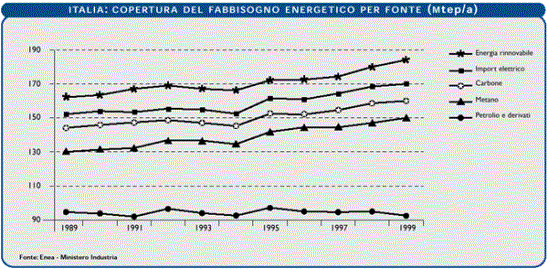
Fig.7
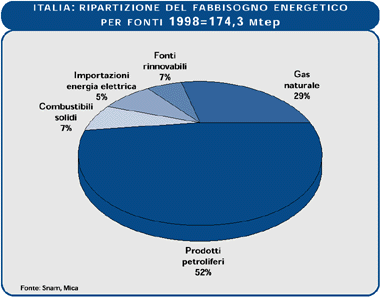
Fig.8