ESERCIZIO
NUMERICO _ Relativo al CICLO CLASSICO FRIGORIFERO (miscele d’acqua e vapor
d’acqua)
v
CONOSCENZE PRELIMINARI:
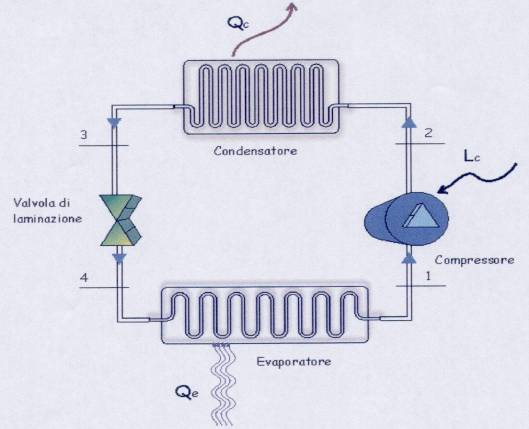
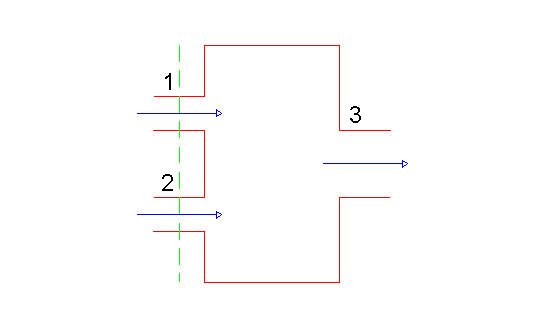
La macchina frigorifera è composta da quattro sistemi aperti che, collegati tra loro, generano un sistema chiuso.
- COMPRESSORE: macchina che opera una compressione adiabatica del liquido e necessita di una certa energia esterna (lavoro Lc) per poter funzionare (questo azionamento è generalmente effettuato tramite motori elettrici).
L’energia spesa dal compressore si trasferisce nel gas evolvente che si surriscalda rispetto alla temperatura di saturazione aumentando anche la sua pressione.
- CONDENSATORE: macchina che compie una trasformazione isobara del liquido che viene raffreddato.
Il refrigerante, mantenendo costante la pressione, si condensa totalmente passando dallo stato gassoso a quello liquido ed essendo stato raffreddato rilascia una certa quantità di calore ( Qe ).
- VALVOLA DI LAMINAZIONE: può essere costituita da una valvola (valvola di strozzatura, come nel caso del seguente esercizio) oppure da un tubo di piccolo diametro (tubo capillare).
Questa valvola permette al liquido refrigerante di effettuare una espansione isoentalpica, considerata irreversibile anche nei cicli ideali.
|
|
|
|
|
|
|
|||||||||||||||
|
T
2 1 4 3 S
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||
|
50 |
3 |
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||
|
40 |
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||
|
5 |
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
S |
|
|||||||||||||||
|
|
|
|
|
|
|
COMFORT
TERMO – IGROMETRICO (ovvero quale deve essere la condizione dell’ambiente per
avere una situazione di piacevolezza dal punto di vista fisico)
Possiamo avere vari tipi di comfort che generano una situazione piacevole all’interno di un ambiente:
- Termo-igrometrico (termodinamica);
- Visivo (illuminotecnica);
- Acustico (acustica applicata);
- Vibrazionale (meccanica applicata);
- Olfattivo (termofluidodinamica);
- Tattile (legata al design).
Quello da noi preso in considerazione è il comfort termoigrometrico che coinvolge e lega tra loro due grandezze fondamentali per l’abitabilità dell’ambiente:
PMV: voto medio
previsto
Se –0,5 < PMV < 0,5 si verifica una situazione di scostamento
normalizzata rispetto alle condizioni di comfort.
Meno del 10% dei soggetti è insoddisfatto
│PMV│< 0,5 questa diventa la condizione di progetto
poiché le condizioni poste si sono rivelate adatte a creare un ambiente
ospitale.
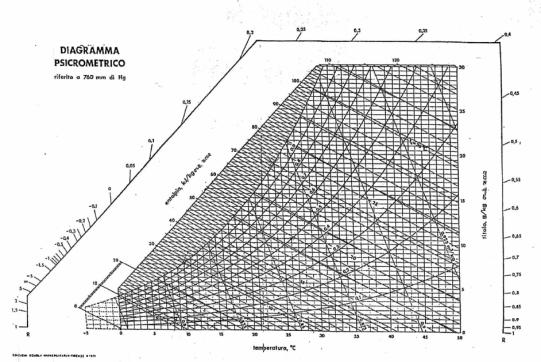
Un’altra sperimentazione interessante è quella fatta da ASHRAE che
studia le condizioni di comfort ottimali basandosi su diagrammi per condizioni
reali.
Questo metodo prende in considerazione
condizioni medie, di moderato vestimento e media attività ma può comunque
essere utilizzato per condizioni più estreme.
Esistono molte tabelle empiriche ricavate in
base a teorie più o meno efficaci e soprattutto in base a rilievi sperimentali,
ovvero testate su varie persone, che permettono di decidere quali devono essere
gli intervalli di temperatura e di umidità entro cui bisogna rimanere per
mantenere il locale vivibile e piacevole.
Queste tabelle si basano soprattutto su una teoria che considera il
corpo umano come un sistema aperto, quindi un sistema che scambia calore con
l’esterno.
Partendo da questi presupposti possiamo scrivere:
EQUAZIONE DEL BILANCIO ENERGETICO DEL CORPO UMANO:
∑ Mi ( lci + lpi + hi ) = Q – L
ESERCIZIO
NUMERICO _ Relativo ad EMISSIONI D’ARIA e VAPOR ACQUEO
v CONOSCENZE PRELIMINARI:
TITOLO : X = –––– ( kgv / kga ) ed esprime il rapporto tra massa d’aria e vapore.
Ma
Mvs: massa di vapore di saturazione.
Data una massa di vapore Va esiste una particolare Mvs in grado di saturarla; un ulteriore apporto d’acqua non evapora oppure si condensa sulle pareti, ritornando liquido. All’aumento di temperatura serve più vapore di saturazione e viceversa. Per T « 0 diminuisce ma non è mai nullo; si annulla solo allo 0 kelvin mentre per T vicine a 100°C tende a ∞.
Vtot ntot Mv / μv + Ma / μ
Con:
μa = 29 kg / kmol
μv = 18 kg / kmol
UMIDITA’ RELATIVA (o grado idrometrico):
per umidità relativa si intende il rapporto tra masse mentre per grado idrometrico il rapporto tra pressioni.
Mv Pv
Φ = ——
≈ ——
Mvs Pvs
Equazione che lega titolo e grado igrometerico:
φ Pvs
X = 0,622 ——————
Ptot – φ Pvs
ESERCIZIO
Dati: Determinare:
Aria umida a T= 30°C Titolo: X
φ= 0,6 (60%) Pv: pressione parziale del
P= 1 BAR (pressione dell’ambiente) vapore
Situazione climatica estiva della Pianura Padana.
Dalla definizione di umidità relativa o di grado idrometrico si ha:
Mv massa vapore μv n. moli vapore
Φ = —— ( ————————— ) = —— ( ————————— )
Mvs massa vapore saturo μvs n. moli vapore saturo
Poiché il vapor d’aria e il vapor d’acqua sono assimilabili ad un gas perfetto possiamo scrivere l’equazione dei gas perfetti:
Pv ![]() V = μv
V = μv![]() R0
R0 ![]() T
T
Con:
Pv = pressione vapore;
V = volume;
μv = numero di moli del vapore;
R0 = costante universale dei gas;
T = temperatura assoluta.
In situazioni di saturazione, l’equazione diventa:
Pvs ![]() V = μvs
V = μvs ![]() R0
R0 ![]() T
T
Pv
Φ = ——
Pvs
Da cui ricaviamo:
Pv = φ ![]() Pvs = 0,6
Pvs = 0,6 ![]() 0,04241 = 2545 Pascal
0,04241 = 2545 Pascal
Dobbiamo ora ricavare il titolo assoluto.
Sappiamo che:
Mv massa volume μv ![]() nv
nv
X = —— ( —————— ) = ————
Ma massa aria μa ![]() na
na
E che μv e μa sono noti quindi il loro rapporto è costante e vale sempre 0,622; possiamo quindi riscrivere la formula in questi termini:
Pv φ ![]() Pvs
Pvs
0,622 ———— = 0,622 ——————
Ptot –
Pv Ptot – φ ![]() Pvs
Pvs
In valori numerici:
0,025446
0,622 —————— = 0,0162
1 – 0,025446
g (di vapore)
che equivale a 16,24 —————
kg (d’aria)