 IL SECONDO PRINCIPIO DELLA TERMODINAMICA
IL SECONDO PRINCIPIO DELLA TERMODINAMICA
Possiamo dire che tutte le ENERGIE sono uguali dal punto di vista quantitativo, cioè tutte si misurano in JOULE (J), ma molto diverse dal punto di vista qualitativo e quindi, di conseguenza anche per quello che riguarda il loro valore economico.
L’energia qualitativamente più elevata è l’ENERGIA ELETTRICA, questa sua importante caratteristica le è data dalla sua alta CONVERTIBILITA’.
Per
convertibilità si intende la possibilità di trasformare l’energia in lavoro (ad
esempio posso trasformare l’energia elettrica, attraverso un motore elettrico,
in movimento). Si può dire quindi, per le sue caratteristiche, che l’energia
elettrica è una ottima fonte primaria.
E’
stato definito in conseguenza a queste osservazioni il concetto di RENDIMENTO DI CONVERSIONE (h):
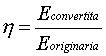 (1)
(1)
Dove h non assume mai valore 1 poiché l’energia convertita sarà sempre minore dell’energia originaria.
Con
questa affermazione non vado contro il Primo principio della termodinamica
(l’energia non si crea e non si distrugge), perché affermo invece che ogni
processo di conversione porta con sé sempre dei processi dissipativi, parte
dell’energia originaria quindi viene dissipata e non è utile per ottenere il lavoro finale, non scompare ma
provoca dei mutamenti nell’ambiente circostante (es. il riscaldamento della
macchina).
Naturalmente per il primo principio della termodinamica avrò sempre:
E originaria
= E convertita + E dissipata
Quindi avrò l’energia convertita nella forma che desideravo e l’energia dissipata che non si è persa o distrutta.
Sarà quindi schematicamente:
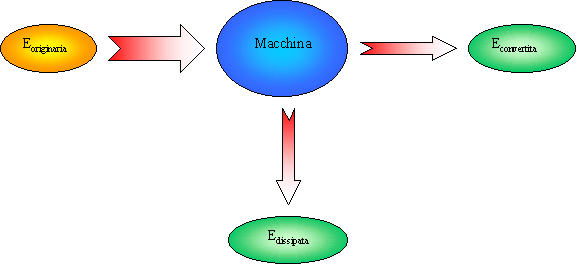
Fig.1 Conversione dell’energia
Sarebbe molto comodo NON avere energia dissipata perché questa non è utile al nostro scopo e inoltre riscalda l’ambiente.
Abbiamo
detto che se l’energia originaria è calore la sua convertibilità è molto bassa
rispetto ad una “energia nobile” come l’energia elettrica.
Avremo
infatti:
Per
il CALORE h<<
1 Cioè il rendimento di
conversione massimo
molto
minore di 1, quindi l’energia convertita
che posso
ottenere è molto minore di quella
originaria.
Per
l’ ENERGIA ELETTRICA
h tende a 1 Cioè l’energia convertita tende
a essere il 99% dell’energia
elettrica originaria.
Possiamo quindi distinguere grazie al rendimento di conversione energie di serie A e di serie B, nobili e meno nobili.
Data infatti una dose di energia, supponiamo 100 J, possiamo ottenere schematicamente:
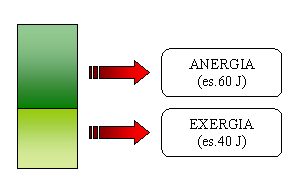 Fig.2 Frazione dell’energia
Fig.2 Frazione dell’energia
Una quota di energia si fraziona quindi in:
-
EXERGIA
che è l’energia di qualità
-
ANERGIA
che è l’energia dannosa scaricata nell’ambiente
Prendendo ad esempio l’energia
elettrica e, come abbiamo detto, la sua alta convertibilità, si può dire che
coincida pressappoco con l’exergia, e che invece l’anergia tenda a zero.
Lo stesso discorso è valido anche per l’energia cinetica e l’energia meccanica, quasi completamente exergetiche.
Da questa proprietà dipende molto anche il
valore di mercato che viene però sbalestrato dalle tasse.
(Un buon progettista deve tenere presente che le
scelte energetiche effettuate in una città non sono per forza adatte a tutte le
altre, questo perché diverse sono le aziende che gestiscono l’energia.)
ENUNCIATO DEL SECONDO PRINCIPIO DELLA TERMODINAMICA
(Prima forma,enunciata da Lord Kelvin)
Sancisce quale è il limite di conversione dell’ENERGIA TERMICA nelle altre energie in relazione alla TEMPERATURA.
Ricordiamo che: l’energia termica NON è
convertibile con un rendimento di conversione simile a 1.
Questo concetto è esprimibile anche attraverso
un paradosso:
IL MOTO PERPETUO
Che può essere di tre specie:
-1° SPECIE:è un sistema che senza alcun apporto dall’esterno
produce lavoro. Questo significherebbe che l’energia scaturisce dal niente ma
si violerebbe il Primo Principio della Termodinamica.
-2° SPECIE:è un sistema a cui forniamo calore e che produce la
stessa quantità di Joule. Schematicamente
 Fig.3 Moto perpetuo di 2°specie
Fig.3 Moto perpetuo di 2°specie
Questo non è possibile per il calore ma è possibile per le altre energie. Chi lavora a questo sistema ritiene che dando calore non dissipo niente.
Il moto perpetuo di seconda specie violerebbe il Secondo Principio della Termodinamica che sancisce un rendimento di conversione molto più piccolo di 1.
-3°
SPECIE:è un sistema dove non
si produce lavoro (cioè non do energia, non ne tolgo e il sistema continua a
girare). Esempio sarebbe una ruota che gira senza attriti. Questo sistema
esiste ed è il moto della TERRA, ma noi non riusciamo a realizzarlo perché non
riusciremmo a togliere tutti gli attriti. In questo sistema il lavoro uscente è
nullo.
Questo era stato intuito da Newton nel Principio di Inerzia (un corpo continua nel suo stato iniziale di quiete o di moto con velocità costante a meno che sia soggetto all’azione di una forza esterna), anche se ancora non gli era noto il concetto di energia.
ENUNCIATO DEL SECONDO PRINCIPIO DELLA TERMODINAMICA
(Seconda forma, enunciata da Clausius)
Consideriamo
un serbatoio a temperatura T1 costante che fornisce calore Q1
e riscalda l’ambiente.
Ricordiamo che per serbatoio si intende un sistema in cui è in atto un cambiamento di fase a temperatura costante, ad esempio una pentola in cui l’acqua bolle a 100° C.
Schematicamente
sarà:
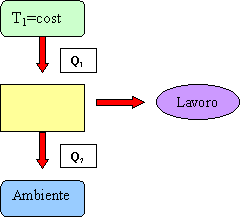 Fig.4 Sistema
diretto tra due serbatoi
Fig.4 Sistema
diretto tra due serbatoi
Supponiamo adesso di poter disporre di una macchina REVERSIBILE che risulterà schematicamente:
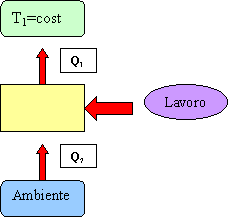 Fig.5 Sistema inverso :macchina
frigorifera
Fig.5 Sistema inverso :macchina
frigorifera
Quella
che ho ottenuto è la MACCHINA
FRIGORIFERA, in cui sfruttando la reversibilità riesco ad estrarre
calore Q2 da una sorgente fredda
T2 per cederla ad una sorgente più calda T1
, ricordiamo infatti che T2<T1.
Arrivati
a questo punto possiamo dire che la seconda forma dell’enunciato del secondo
principio della termodinamica nega la possibilità di avere una macchina
frigorifera capace di trasportare da un ambiente freddo ad uno caldo, calore,
senza avere energia (Lavoro L) dall’esterno.
E’
stato stabilito quindi un consumo minimo (Lmin) pari al 30%.
LA MACCHINA DI CARNOT
Abbiamo
notato che per il Secondo Principio della Termodinamica non è possibile avere
una macchina che opera tra due serbatoi di calore a temperatura T1 e
T2 costante con un rendimento del 100%.
Ci
chiediamo quindi adesso quale può essere il massimo rendimento possibile per
questo tipo di macchine.
A
questa domanda diede risposta a metà dell’800 SADI CARNOT, 50 anni prima
dell’enunciato del Secondo principio della Termodinamica di Kelvin e Clausius.
Carnot
definì il rendimento di conversione
come COEFFICIENTE
ECONOMICO DELLA MACCHINA A VAPORE ![]()
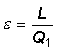 (2)
(2)
Dove
troviamo ancora un rapporto tra l’energia convertita (L) e l’energia originaria
(Q1).
Ricordiamo
che per MACCHINA A VAPORE intendiamo tutte quelle macchine che operano tra due
serbatoi di calore che agiscono a temperature costanti.
Studiando
proprio le macchine a vapore Carnot formulò il suo teorema:
Nessuna macchina a vapore che lavori tra
due termostati può avere un
rendimento maggiore di una macchina
reversibile che lavori tra questi due
stessi termostati.
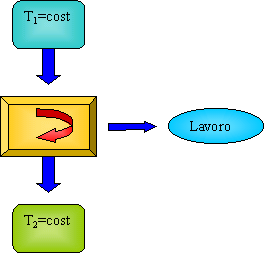 Fig.6 Macchina ciclica
Fig.6 Macchina ciclica
Questa è una MACCHINA CICLICA, cioè considerando un numero intero di cicli la macchina torna al suo stato iniziale.
Da
questo posso quindi sfruttare il Primo Principio della Termodinamica che mi
dice:
Q1 = Q2 + L (3)
quindi
sarà
L
= Q1 – Q2
Andando poi a sostituire ciò che ho trovato nella formula del coefficiente economico otterrò:
![]() (4)
(4)
Carnot
però desidera ottenere la macchina (definita MACCHINA DI CARNOT) con il più alto coefficiente
economico e quindi ottenne:
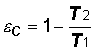 (5)
(5)
Si
può notare come il rapporto tra le quantità di calore scambiata sia uguale al
rapporto tra le temperature nei serbatoi.
Grazie
a questa formula riusciamo a quantificare la frazione di energia convertibile
in lavoro.
ESERCIZIO
Abbiamo a
disposizione in un serbatoio un
quantità di energia pari a 1000 J (Etot=1000J)
ad una temperatura T1=300° C
Vogliamo conoscere
quanto sarà l’exergia (Ex)
Consideriamo come
temperatura ambiente T2=20°C
Dalla formula del
coefficiente economico ottengo:
![]()
Prima di tutto devo
trovare il rendimento di Carnot che sarà dato da:
![]()
Devo ricordarmi che T1
e T2 devono essere
trasformate secondo il Sistema Internazionale in gradi Kelvin quindi avrò:
T1 = 300° C = 573 K T2 = 20° C =293 K
Possiamo quindi
risolvere:
![]()
Sostituisco
adesso il valore trovato di ec =0,488
nella formula del coefficiente economico per ottenere in questo modo ciò che
cercavamo cioè l’exergia:
![]()
A
questo punto si può anche trovare facilmente l’anergia cioè la quota di energia
dissipata (Q2), infatti:
![]()
quindi
![]()
Da
questo esercizio possiamo vedere che maggiore è il divario tra le due
temperature (secondo le nostre formule, maggiore sarà T1) e più
elevato sarà il rendimento di conversione.
Quindi
Il rendimento di conversione del calore VARIA a seconda della temperatura a cui si trova.
LE POMPE DI CALORE
Nel riscaldamento invernale di un locale abitativo o pubblico il fine da raggiungere è quello di portare la temperatura del locale ad una temperatura sensibilmente maggiore di quella dell’ambiente esterno.
Il
procedimento normalmente usato è quello di fornire calore per mezzo di acqua
calda circolante nei radiatori, acqua che è stata riscaldata per combustione di
nafta, gasolio o metano. Oppure, procedimento comune è quello di usare una
stufa elettrica in cui energia elettrica è trasformata direttamente in calore
ceduto al locale mediante dissipazione di Joule.
Questi
metodi sono ben poco efficienti perché portano all’aumento di temperatura attraverso una degradazione totale
dell’energia meccanica o chimica consumata.
Per
sfruttare l’energia elettrica di una stufa nel metodo termodinamicamente più
conveniente, essa dovrebbe essere impiegata per operare un ciclo frigorifero il
più efficiente possibile, con il quale si trasferisca calore dall’ambiente
esterno, più freddo, al locale da riscaldare in inverno e che faccia il lavoro
opposto in estate.
Le
macchine frigorifere che vengono utilizzate per trasferire calore
dall’ambiente esterno più freddo (il
serbatoio a temperatura minore) ad un altro ambiente a temperatura maggiore,e
viceversa , sono note come POMPE
DI CALORE.
Un esempio è il CONDIZIONATORE che schematicamente sarà:
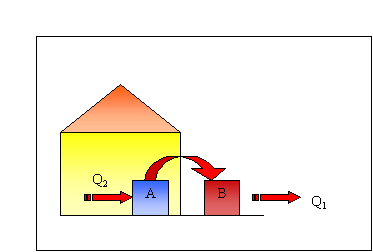
Fig.7
Condizionatore
In
questo caso succederà che A prende il calore Q2 e passando il calore
a B si raffredda, mentre B, a sua volta
si scalderà espellendo il calore Q1 .
A
questo punto possiamo quindi definire il rendimento estivo di questa macchina (hest)
che sarà :
![]()
![]()
(6)
Allo
stesso modo quando la pompa di calore fa il ciclo opposto potrò definire un rendimento invernale (hinv).
![]() (7)
(7)
Schematicamente questa macchina sarà:
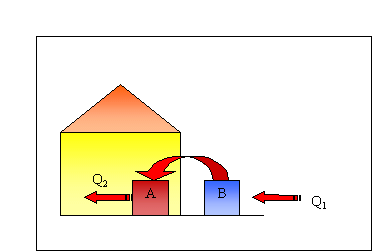
Fig.8 Pompa di calore
In questo caso accadrà che B si raffredda e prende il calore Q dall’ambiente esterno più freddo , lo trasferisce poi ad A che riscaldandosi scalderà anche l’interno dell’abitazione.
Abbiamo visto così che con le pompe di calore posso ottenere due risultati: il freddo se sfrutto il serbatoio a cui sottraggo calore e caldo sfruttando quello a cui fornisco calore e posso così definire due nuove variabili hest e hinv.
Adesso
possiamo cercare di trovare una relazione tra le due nuove variabili se
consideriamo la nostra macchina una macchina di Carnot . Infatti avremo:
![]() (8)
(8)
Cioè
ne deduco che il rendimento invernale hinv
è sempre
migliore del rendimento estivo hest
.
TELERISCALDAMENTO E COGENERAZIONE
Teleriscaldamento:
è una nuova forma di sfruttamento dell’energia che consiste nella distribuzione
del calore da una o più centrali termiche che con una rete di tubi sotterranei
riscaldano tutte le case. Questo tipo di energia è ecologica e permette di
risparmiare sul riscaldamento comune.
Permette
un risparmio energetico annuo di 133 mila tonnellate di petrolio. Una unica
centrale collega più utenti grazie a tubi di nuova generazione, questo
garantisce rendimenti elevati e minor inquinamento termico.
Il
teleriscaldamento si basa sulla centrale normalmente alimentata da metano che fornisce acqua calda
producendo contemporaneamente energia elettrica e calore.
Alla
caldaia viene sostituito uno scambiatore di calore allacciato alla rete di
teleriscaldamento. L’utente paga il calore in base al consumo effettuato.
I
vantaggi sono: l’eliminazione della caldaia, della canna fumaria e dei relativi
costi di manutenzione, sicurezza contro rischi di esplosione e incendi ,
risparmio energetico e minore inquinamento dell’aria.
Cogenerazione
:è la produzione contemporanea di energia termica e
meccanica, quest’ultima subito convertita in energia elettrica tramite un
sistema integrato detto “energia totale”.
I
due tipi di energia sono prodotti separatamente sommando così le perdite di
efficienza. Nel produrre energia elettrica da combustibile, proprio a causa di
perdite di efficienza nella produzione e nel trasporto, all’utente finale
giunge il 35 % dell’energia primaria.
La
produzione di energia termica con caldaie ha attualmente un rendimento del 85%.
Lo scopo della cogenerazione è quello di recuperare le perdite di efficienza
ottenendo mediamente un risparmio superiore
al 35% di energia primaria del combustibile e nello stesso tempo si
ottiene una equivalente riduzione di emissioni di CO2.
Un
sistema di cogenerazione può fornire:
-energia
elettrica;
-acqua
calda per servizi sanitari;
-acqua
calda per riscaldamento di piscine o vasche;
-acqua
calda per riscaldamento dell’ambiente;
-acqua
surriscaldata;
-vapore
per vari usi;
-aria
condizionata.
Un
esempio: BRESCIA
L’ASM è l’azienda che gestisce a Brescia il servizio di teleriscaldamento, che consiste nella fornitura di calore agli edifici in forma di acqua calda mediante una rete di distribuzione sotterranea. Il calore è prodotto congiuntamente all’energia elettrica in 2 centrali.
Inoltre
dal 1998 si è aggiunto un impianto di termoutilizzazione dei rifiuti che è in
sostanza una centrale di cogenerazione alimentata dai rifiuti anziché dai
consueti combustibili fossili. L’impianto soddisfa 1/3 del fabbisogno di calore
della città.
La
rete di teleriscaldamento, avviata nel 1972, consente di riscaldare il 60 % degli
edifici.