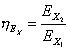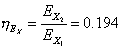IL SECONDO
PRINCIPIO DELLA TERMODINAMICA
PRIMO
PRINCIPIO
: Equivalenza e conservazione
dell’ energia
SECONDO
PRINCIPIO
: Limiti
alla conversione fra energia “vile” e “nobile”
Il primo
principio della termodinamica è semplicemente la legge di conservazione
dell’energia generalizzata per includere il calore come forma di energia.
Questo principio ci dice che un aumento in una delle forme di energia deve
essere accompagnato da una diminuzione di qualche altra forma di energia. Il
primo principio non pone alcuna restrizione sui tipi di conversione di energia
che possono avere luogo; inoltre, esso non fa alcuna distinzione fra calore e
lavoro, Secondo il primo principio, 1’energia interna di un corpo può
essere aumentata sia fornendo calore che eseguendo del lavoro su di esso. Ma
c’e una differenza importante fra calore e lavoro che non è evidente dal
primo principio. Per esempio, è possibile convertire lavoro completamente in
calore, ma, in pratica, è impossibile convertire calore completamente in
lavoro senza produrre delle modifiche nell’ambiente circostante. Il secondo
principio della termodinamica, stabilisce quali processi possano o non possano
avvenire in natura. Di tutti i processi permessi dal primo principio, solo
certi tipi di trasformazioni di energia possono avere luogo. I seguenti sono
alcuni esempi di processi che sono consistenti con il primo principio della
termodinamica, ma possono avvenire solo in un ordine regolato dal secondo
principio della termodinamica.
1
Quando due oggetti a temperature diverse sono messi a contatto termico fra
loro, il calore si trasferisce dall’oggetto più caldo all’oggetto più
freddo, ma mai da quello più freddo a quello più caldo.
2
Quando una palla di gomma è lasciata cadere per terra, rimbalza parecchie
volte ed alla fine si ferma. Il processo opposto non avviene.
3
Le oscillazioni di un pendolo diminuiranno lentamente d’ampiezza a causa
degli urti con le molecole d’aria e dell’attrito sul punto di sospensione.
Alla fine il pendolo si ferma. Pertanto 1’energia meccanica iniziale del
pendolo è convertita in energia termica. Il processo inverso non avviene.
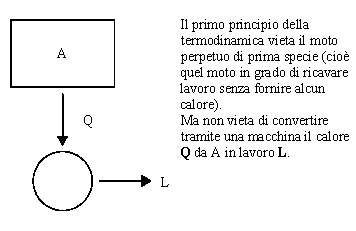
Fig.
1
Il
Secondo principio della termodinamica, che può essere enunciato in
molti modi diversi, ha applicazioni molto pratiche. Dal punto di vista
dell’ingegneria, forse 1’applicazione più importante è 1’efficienza
limitata delle macchine termiche.
Enunciato
semplicemente, il secondo principio dice che una macchina capace di convertire
con continuità energia termica completamente in altre forme di energia non può
essere costruita.
Altri
enunciati del secondo principio della termodinamica sono:
Nessuna
macchina termica che funzioni con un ciclo può assorbire energia termica da
un serbatoio e produrre una eguale quantità di calore (Enunciato
di Kelvin-Planck)
E’
impossibile costruire una macchina a moto perpetuo di seconda specie.
E’
impossibile costruire una macchina ciclica il cui unico effetto sia il
trasferimento continuo di calore da un corpo ad un altro a temperatura più
alta. (Enunciato di
Clausius)
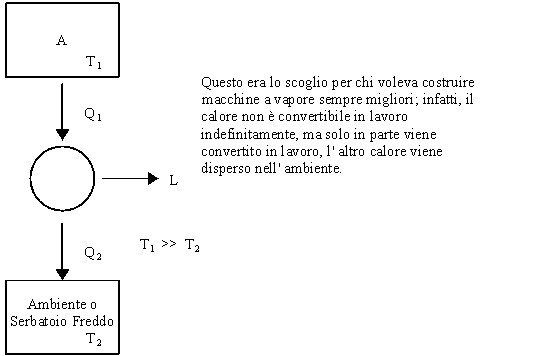
Fig.
2


Fig.
3
Lord Kelvin, fisico e matematico inglese(1824-1907)
Fig.
4
Rudolph Clausius(1822-1888)
Una Macchina termica è un dispositivo che trasforma energia
termica in altre forme utili di energia, come 1’energia meccanica ed
elettrica. Più specificatamente una macchina termica è un dispositivo che fa
compiere ad una sostanza un ciclo durante il quale:
1
Il calore viene assorbito da una sorgente ad alta temperatura,
2 Del lavoro viene eseguito dalla macchina e
3 Il calore è ceduto dalla macchina ad una sorgente a temperatura più
bassa.
In un tipico processo per produrre elettricità in una centrale
elettrica, si sottopone carbone o altri carburanti ad un processo di combustione
e il calore prodotto viene usato per convertire 1’acqua in vapore. Questo
vapore viene poi diretto sulle eliche di una turbina che si mette in rotazione.
Infine, 1’energia meccanica associata a questa rotazione è usata per azionare
un generatore di corrente.

Fig.
5
Modello
di Macchina a vapore a caldaia orizzontale. L’acqua riscaldata elettricamente
produce il vapore che fornisce potenza al generatore di energia elettrica di
destra
Il motore a combustione interna della nostra auto assorbe calore dalla
combustione del carburante e converte una frazione di questa energia in energia
meccanica. Come detto prima, una macchina termica fa compiere ad una sostanza
una trasformazione ciclica, la quale viene definita come una trasformazione alla
fine della quale la sostanza ritorna allo stato iniziale. Come esempio di
trasformazione ciclica, si consideri il modo di funzionare di un motore a vapore
in cui la sostanza che lavora è 1’acqua. Si fa compiere all’acqua un ciclo
in cui essa prima si trasforma in vapore in un bollitore, e poi si espande
contro un pistone. Successivamente il vapore viene condensato con dell’acqua
di raffreddamento, viene rimandato al bollitore, ed il processo viene ripetuto.
Nel funzionamento di qualsiasi macchina termica, si assorbe una quantità di
calore da una sorgente a temperatura alta, si fa del lavoro meccanico e si cede
del calore ad un serbatoio a temperatura bassa. (Fig. 2)
Per vedere quanto siano efficaci queste macchine termiche, definiamo il Coefficiente
Economico come:
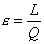 Eq.
1
Eq.
1
dove L è il lavoro prodotto, mentre Q rappresenta il
calore speso per ottenerlo.
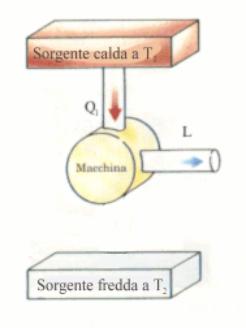
Fig.
6
Macchina
termica con efficienza perfetta impossibile da realizzare
Si può pensare al coefficiente economico (o rendimento) come al
rapporto fra “ciò che si ottiene” (lavoro meccanico) e “ciò con cui si
paga” (calore).
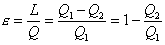 Eq.
2
Eq.
2
Questo risultato mostra che una macchina termica ha rendimento pari al
100%, cioè e=1,
solo se
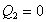 ,cioè solo se non viene ceduto calore al serbatoio freddo.
,cioè solo se non viene ceduto calore al serbatoio freddo.
In altre parole una macchina termica con efficienza perfetta dovrebbe
convertire tutto il calore assorbito
 in lavoro. Ma il secondo principio
della termodinamica dice che questo è impossibile!!
in lavoro. Ma il secondo principio
della termodinamica dice che questo è impossibile!!
Questo
vuol dire che è impossibile costruire una macchina a moto perpetuo di seconda
specie. (Cioè un sistema che converta tutto il calore in lavoro)
TRASFORMAZIONI REVERSIBILI ED IRREVERSIBILI
Sopra si era detto che le traformazioni reali hanno una direzione
privilegiata: il calore fluisce spontaneamente da un corpo caldo ad uno freddo
quando si mettono i due corpi a contatto, mentre il processo inverso per
avvenire ha bisogno di una qualche influenza dall’ esterno (lavoro). Le
trasformazioni unidirezionali sono irreversibili. In generale, una
trasformazione è irreversibile se il sistema e l’ambiente non possono
essere fatti tornare al loro stato iniziale. Una trasformazione è invece reversibile
se un sistema passa dallo stato iniziale a quello finale attraverso una
successione di stati d’equilibrio. Questo vuol dire che se una trasformazione
avviene quasi staticamente, cioè abbastanza lentamente in modo tale che
ciascuno stato differisca solo infinitesimamente dall’ equilibrio, può essere
considerata reversibile. Inoltre, in una trasformazione reversibile non ci
debbono essere effetti dissipativi che producano calore. (In natura è alquanto
improbabile che ciò avvenga)
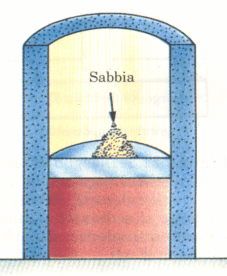
Fig.
7
Esempio di
trasformazione reversibile: se si immagina di comprimere un gas quasi
staticamente lasciando cadere dei granelli di sabbia lentamente su un pistone
senza attrito, la temperatura, la pressione ed il volume sono ben definiti
durante la compressione (che è isoterma). La trasformazione è resa isoterma
mantenendo il gas a contatto termico con un serbatoio di calore. Ogni volta che
un granello di sabbia viene aggiunto al pistone, il volume diminuisce
leggermente mentre la pressione aumenta pure leggermente. La trasformazione può
essere rovesciata rimovendo altrettanto lentamente i granelli di sabbia dal
pistone.
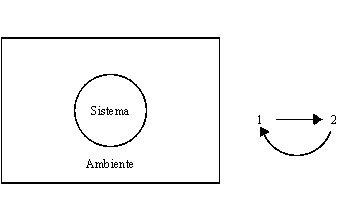
Fig.
8
La
trasformazione è reversibile solo se il sistema e l’ambinte passati dallo
stato 1 allo stato 2, ritornano allo stato 1 (cioè quello iniziale)
TEOREMA DI CARNOT
Nel 1824 il fisico francese Sadi Carnot descrisse un ciclo di lavoro,
ora detto , il ciclo di Carnot quale diverrà di notevole importanza sia
dal punto di vista pratico che teorico. Carnot dimostrò che una macchina
termica che funzionasse con questo ciclo reversibile ideale fra due serbatoi di
calore, sarebbe la macchina più efficace possibile. Questa macchina ideale ,
detta macchina di Carnot, stabilisce un limite superiore irraggiungibile
e quindi insuperabile per i rendimenti di tutte le macchine. Cioè il lavoro
complessivo fatto da una sostanza che compie il ciclo di Carnot è il massimo
che può essere ottenuto da una data quantità di calore fornita alla sostanza
utilizzata nella macchina. Il teorema di Carnot può essere così
enunciato:
Nessuna
macchina termica reale operante tra due serbatoi di calore può essere più
efficiente di una macchina di Carnot operante tra gli stessi due serbatoi.
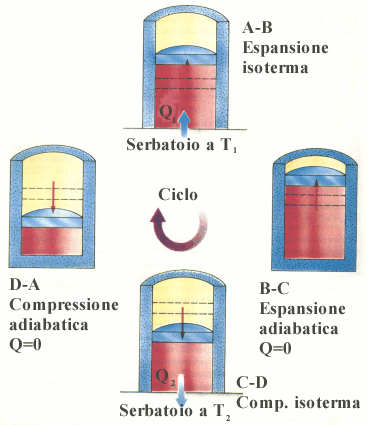
Fig.
9
Il ciclo di
Carnot. (Si ipotizza venga effettuato con granelli di sabbia lasciati cadere sul
pistone)
Per descrivere il ciclo di Carnot si assume che la sostanza operante tra
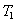 e
e
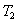 sia un gas perfetto contenuto in un
cilindro con un pistone mobile all’estremità. Le pareti del cilindro ed il
pistone sono termicamente isolanti, ed il ciclo si compone di due trasformazioni
adiabatiche e due trasformazioni isoterme come da Fig.
9.
sia un gas perfetto contenuto in un
cilindro con un pistone mobile all’estremità. Le pareti del cilindro ed il
pistone sono termicamente isolanti, ed il ciclo si compone di due trasformazioni
adiabatiche e due trasformazioni isoterme come da Fig.
9.
Il
lavoro complessivo fatto da questo processo ciclico reversibile è uguale
all’area racchiusa dal cammino ABCDA del diagramma PV di Fig.
10.
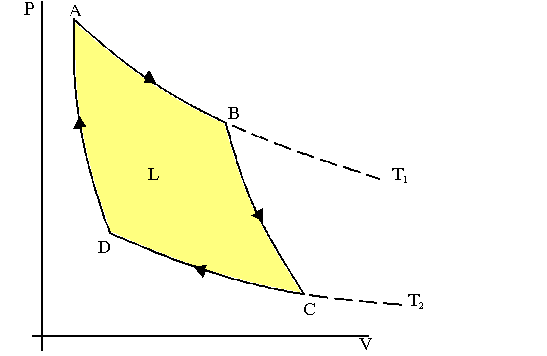
Fig. 10
Il
lavoro complessivo fatto in un ciclo è uguale al calore scambiato dal sistema,
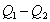 , questo in quanto la variazione di energia interna è nulla. Quindi il
coefficiente economico della macchina è dato dalla stessa equazione di prima:
, questo in quanto la variazione di energia interna è nulla. Quindi il
coefficiente economico della macchina è dato dalla stessa equazione di prima:
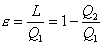 Eq. 3
Eq. 3
Si
dimostra (non in questa sede) che in un ciclo di Carnot il rapporto dei calori
è lo stesso delle temperature:
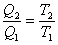 Eq. 4
Eq. 4
Quindi,
il coefficiente economico di una macchina di Carnot è:
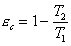 Eq. 5
Eq. 5
Riassumendo possiamo dire che il pimo principio permetteva
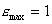 Eq. 7
Eq. 7
ora il secondo principio della termodinamica afferma che
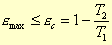 Eq. 8
Eq. 8
Questo
risultato ci porta a fare alcune considerazioni; partiamo con un esempio:
Se
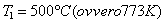 e
e
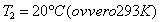 , il coefficiente economico di Carnot sarà dato ovviamente dalla semplice
equazione
, il coefficiente economico di Carnot sarà dato ovviamente dalla semplice
equazione
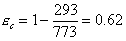 Eq. 9
Eq. 9
Questo
non significa altro che il solo il 62% del calore iniziale è stato convertito
il lavoro, mentre il rimanente 38% è stato ceduto all’ ambiente.
Quindi,
se io avessi avuto all’inizio 1 KJ:
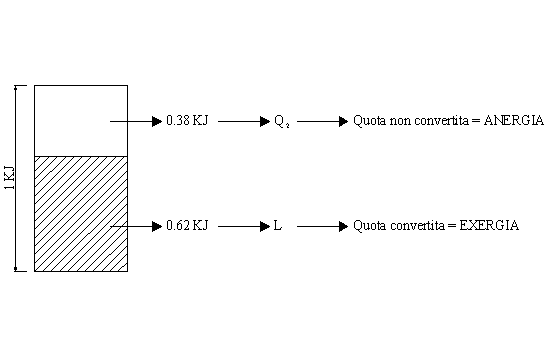
Fig. 11
ANERGIA
ED EXERGIA
Dall’
esempio si capisce come tutte le volte che ho del calore, e voglio trasformarlo
in lavoro, avrò sempre una parte di questo calore “iniziale” che dovrò ”spararlo”
nell’ambiente. D’ora in poi chiameremo la quota di energia o calore sprecato
ANERGIA e la indicheremo
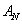 , mentre la quota di energia calore convertita in lavoro la chiameremo EXERGIA
e la indicheremo
, mentre la quota di energia calore convertita in lavoro la chiameremo EXERGIA
e la indicheremo
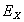 .(Fig. 11)
.(Fig. 11)
Per
concludere le considerazioni precedenti, si vuole chiarire che il coefficiente
economico di una macchina, dipende esclusivamente dalle temperature tra le quali
opera; quindi, se non è una macchina estremamente grossolana o mal realizzata,
questa presumibilmente si comporterà come dice Carnot. Naturalmente non sarà
possibile eguagliare il coefficiente economico di Carnot, ma sarà altrettanto
inutile sforzarsi di costruire macchine sempre migliori, con attriti o altro che
potrebbe ostacolare il processo, sempre più infinitesimali. La cosa principale,
e si ribadisce, sono le temperature tra le quali la macchina lavora!
Ovviamente
l’enrgia totale prima della sua
trasformazione (
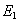 ), sarà uguale all’energia totale dopo la trasformazione (
), sarà uguale all’energia totale dopo la trasformazione (
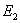 ). Adesso però possiamo dire la “qualità” di questa energia che ho prima e
dopo.:
). Adesso però possiamo dire la “qualità” di questa energia che ho prima e
dopo.:
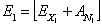 Eq. 10
Eq. 10
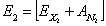 Eq. 11
Eq. 11
Possiamo anche affermare che dopo la trasformazione sarà vera la
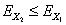 Eq. 12
Eq. 12
Se ora noi definiamo anche il rendimento Energetico come
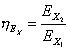 Eq. 13
Eq. 13
possiamo fare un esempio chiarificativo sul valore economico
dell’energia.
Ipotizziamo
di voler scaldare una casa con una resistenza elettrica; sarebbe molto bello,
nessuna caldaia, nessun rischi di scoppio, veramente geniale insomma!
Ma
così facendo, otterremmo un rendimento Energetico molto basso, il che equivale
a dire che dequalificheremmo moltissimo l’ energia. Bisogna valutare molto
bene il valore economico dell’energia, e l’energia elettrica costa molto!!
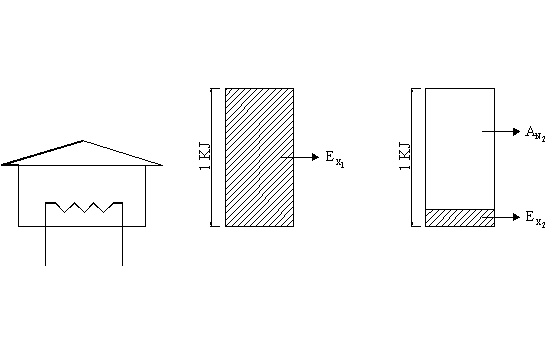
Fig. 12
Prima la nostra energia era tutta Energia,
poi la abbiamo dequalificata producendo Anergia.
Quando
si progetta, quindi, se si vuole fare qualcosa di “diverso”, bisogna tener
conto che non per sempre potrà andare bene, ed è quindi buona cosa progettare
contestualmente una soluzione che sia in futuro facilmente convertibile in
un’altra.
Proviamo
ora a fare un esempio più vicino a noi:
Guardiamo
quanto si dequalifica l’energia quando riscaldiamo la nostra casa con
dall’acqua calda a 60°C immessa nei nostri termosifoni, ipotizzando di non
sprecare calore nel tragitto, che a compiere la trasformazione sia una macchina
di Carnot, e quant’altro ci possa tornare utile affinché non ci siano
disturbi.
I
nostri dati sono quindi:
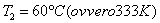 che ipotizziamo siano pari ad 1 kJ
che ipotizziamo siano pari ad 1 kJ
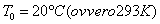 che sarebbe la temperatura della
casa riscaldata.
che sarebbe la temperatura della
casa riscaldata.
(vedi
Fig. 13)
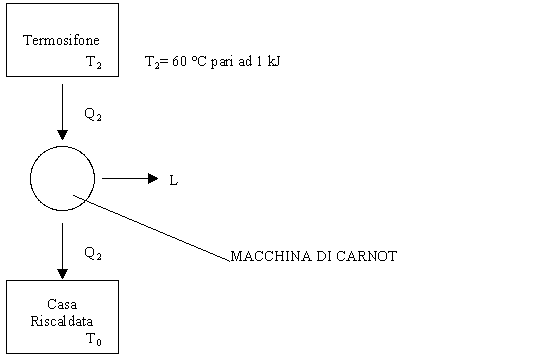
Fig. 13
Ora
noi sappiamo che da 1 kJ con una macchina di Carnot ricaviamo 0.62
kJ di exergia (
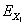 ) e 0.38 kJ di anergia (
) e 0.38 kJ di anergia (
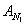 ).
).
Col nostro bel termosifone, le cose saranno:
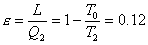 Eq. 14
Eq. 14
(è alquanto basso!)
Questo
vuol dire che dal nostro bel 1 kJ iniziale di “qualità” sopra desritta,
avremo 0.12 kJ di exergia (
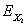 ) e 0.88 kJ di anergia (
) e 0.88 kJ di anergia (
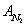 )
)
Quindi
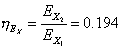 Eq. 15
Eq. 15
(è molto basso anche questo!!!)
POMPE
DI CALORE
Una
pompa di calore è un dispositivo che si sta diffondendo per il riscaldamento ed
il condizionamento di case ed edifici. I nomi commerciali sono rispettivamente
pompa di calore e macchina frigorifera. Ma non c’è assolutamente bisogno di
comprare due macchine distinte, sono esattamente la stessa cosa, cambia solo il
verso di funzionamento. Quando si utilizza per riscaldare, di solito un fluido
circolante assorbe calore dall’esterno e lo cede all’ interno della
struttura. Tale fluido è usualmente un vapore a bassa pressione che, contenuto
in una serpentina al di fuori della struttura, assorbe calore dall’aria o
dalla terra. Il gas viene quindi compresso ed entra nella struttura come vapore
caldo ad alta pressione. All’ interno il gas condensa diventando liquido e
cede l’energia interna accumulata. Quando si utilizza come condizionatore il
ciclo è invertito.
Una
rappresentazione schematica di una pompa di caolore potrebbe essere:
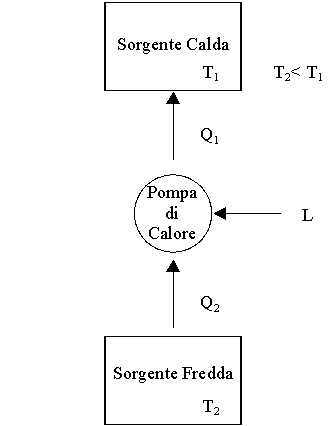
Fig. 14
La temperatura esterna è
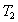 , quella interna è
, quella interna è
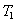 , il calore assorbito dal fluido circolante è
, il calore assorbito dal fluido circolante è
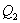 . Un compressore compie il lavoro L sul fluido, ed il calore ceduto alla casa è
. Un compressore compie il lavoro L sul fluido, ed il calore ceduto alla casa è
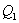 .
.
Ricordiamo
ora che la macchina di Carnot può tornare indietro, cioè è reversibile, e che
una macchina reversibilemantiene lo stesso rapporto
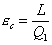 .
.
L’efficienza
di una pompa di calore viene descritta da un numero detto coefficiente di
prestazione, COP. Questo coefficiente è definito come segue:
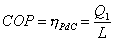 Eq. 16
Eq. 16
Il rendimento di un frigorifero sarà ovviamente invece:
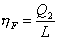 Eq. 17
Eq. 17
Un frigorifero efficiente è un frigorifero che sottrae la maggior
quantità di calore dal serbatoio freddo con la minor quantità di lavoro
possibile. Pertanto un buon frigorifero dovrebbe avere un rendimento piuttosto
alto, tipicamente 4 o 5. Il frigorifero perfetto (impossibile da realizzare)
avrebbe un coefficiente di prestazione infinito
Ricordiamo però dal primo principio della termodinamica che:
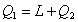 Eq. 18
Eq. 18
Allora:
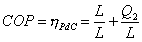 Eq. 19
Eq. 19
Cioè:
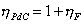 Eq. 20
Eq. 20
Supponiamo di usare 1 kJ di energia elettrica che da il lavoro L,
che
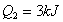 e
e
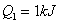 entrambi di energia termica, allora
si avrà che
entrambi di energia termica, allora
si avrà che
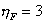 e
e
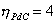 .
.
INQUINAMENTO
TERMICO
La
principale fonte di inquinamento termico è lo spreco di calore delle centrali
elettriche. Il rendimento termico totale di una centrale a carburante fossile
moderna è circa il 40%. I rendimenti reali di qualsiasi centrale elettrica
devono essere più bassi dei rendimenti teorici derivati dal secondo principio
della termodinamica. Si cerca sempre il rendimento più alto per due ragioni:
1
Rendimenti più alti comportano minor costo del carburante.
2
L’inquinamento termico dell’ambiente viene ridotto, perché c’è minor
spreco di energia in una centrale altamente efficiente.
Poiché
qualsiasi centrale comporta parecchi stadi di trasformazione dell’energia,
l’inefficienza si accumula a stadi; la combustione di carburanti fossili in
una centrale elettrica comporta tre processi di trasformazione dell’energia:
1
Da energia chimica ad energia termica
2.
Da energia termica ad energia meccanica
3.Da
energia meccanica ad energia elettrica
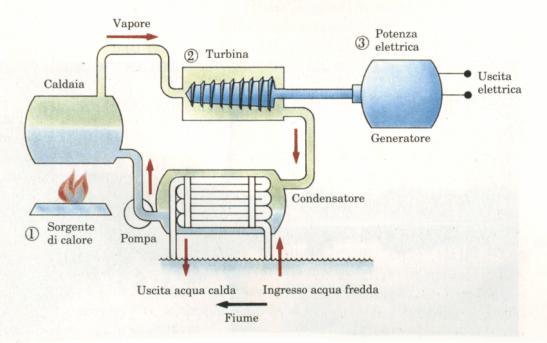
Fig. 15
Come
si può vedere da Fig. 16, si immette nel fiume
acqua calda servita alla condensazione dei vapori. Ma anche così facendo, la
temperatura del fiume salirà di parecchi gradi, il che può produrre effetti
ecologici indesiderati. Anche i pesci ed altre forme di vita ne risentirebbero.
Nel
caso di centrali nucleari, nonostante grazie ai materiali del reattore i vapori
generati siano a temperatura più bassa che quelli di una centrale a carburante
fossile, si utilizzano le torri di raffreddamento per far evaporare acqua che
viene poi immessa nell’atmosfera. Anche le torri presentano problemi
ambientali, poiché l’acqua evaporata può causare aumenti della
precipitazioni, nebbia, ghiaccio. Esistono anche tipi di torri dette di
raffreddamento asciutto (non evaporative), ma a parte il maggior costo, sono
anche meno efficienti nell’abbassare la temperatura.

Fig. 16
Anche
noi, nelle mura domestiche, possiamo e dobbiamo prestare attenzione
all’inquinamento termico che produciamo.
Se
produciamo totalmente il calore per riscaldare la nostra casa, per esempio con
energia elettrica, tutto quello che abbiamo prodotto prima o poi verrà disperso
nell’ ambiente. Se invece “succhiamo” energia dall’esterno in parte, ed
in parte la produciamo, ecco che ciò che viene disperso in realtà in parte
veniva dall’ambiente.
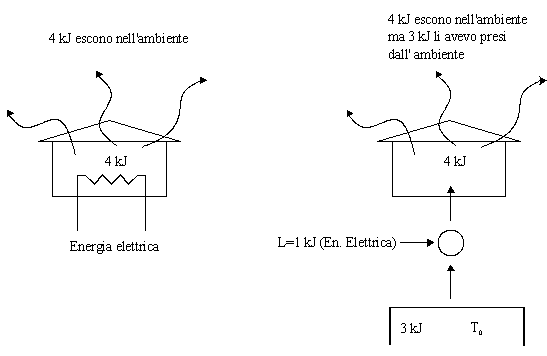
Fig. 17
Fig. 18
Come
si vede da Fig. 18, il risparmio è del 75%!!
……IL TERZO PRINCIPIO…
Non
si possono usare apparecchi domestici per dimostrare il terzo principio della
termodinamica, perchè la sua sfera d’azione è molto più particolare, la
regione del molto freddo, di quella del primo e del secondo principio che
dominano l’intero arco di temperatura. Senza dubbio, la natura esotica di
questo sfera d’azione è la ragione per cui il terzo principio fu 1’ultimo
dei tre a venire proposto, nel 1906, da Walther Nernst, dell’Universita di
Berlino (per cui egli vinse il premio Nobel per la chimica, nel 1920). Precedentemente
i fisici supponevano che, quando molecole e atomi venivano raffreddati
gradualmente rallentassero fino ad arrestarsi, allo zero assoluto. Ma la teoria meccanico-quantistica della materia, che
andava emergendo a fine secolo, non permette ciò. La più bassa energia
disponibile ad un atomo, chiamata energia dello stato fondamentale, non è zero;
rimane sempre una piccola, irriducibile vibrazione, che può essere teoricamente
descritta e misurata sperimentalmente. L’energia associata con questo stato
non può essere spartita con altri oggetti (non puo ”fluire”) o essere
interpretata come calore e quindi non conta come disordine. Ragionando in questo
modo, Nernst arrivò ad un nuovo concetto dello zero assoluto: piuttosto che
un’assenza di moto, esso significa 1’assenza di disordine, o uno stato di
ordine perfetto, e questo diventa la versione iniziale del terzo principio della
termodinamica. Sei anni più tardi, esaminando il calore specifico degli
elementi chimici, Nernst scoprì un fatto interessante: nell’avvicinamento
allo zero assoluto, o all’ordine perfetto, ciascun passo e più difficile del
precedente. La
temperatura, ad ogni succesiva cessione di calore, diminuisce di meno. Egli
trovò che questa relazione non è semplicemente una proprietà casuale di
particolari sostanze ma un attributo di tutta la materia. Attribuendo il
fenomeno alla difficoltà di distribuire un numero enorme di molecole non
soggette a regole in un singolo stato di perfetto ordine (le possibilità sono
astronomiche che per lo meno alcune sfuggiranno alla cattura), Nernst propose
una forma vincolante del terzo principio: lo zero assoluto non è raggiungibile.
Va fatto un confronto con una imposizione simile ma in un contesto diverso:
1’affermazione di Einstein che gli oggetti non possono raggiungere la velocità
della luce. Quando fu proposto per la prima volta, questo principio sembrò
strano, perchè il fenomeno avveniva in assenza di una forza specifica di
compensazione. Ma poi Einstein mostrò che, quando un oggetto accelera, la sua
massa cresce (come riassunto nella formula E = mc²). Da ciò egli
dedusse che, quando un oggetto si avvicina alla velocita della luce, 1’energia
richiesta per una ulteriore accelerazione approssima un valore infinito. Un
cambio di variabili, da velocità ad energia, fece apparire comprensibile un
limite incomprensibile. Analogamente, in modo approssimativo, il passaggio di
Nernst dall’assenza di moto all’assenza di disordine come il fatto
determinante dello zero assoluto, fece apparire la sua dichiarazione plausibile.
Ciò implica che, quando un oggetto si avvicina ad uno stato di ordine perfetto,
lo sforzo richiesto per eliminare il disordine residuo si avvicina
all’infinito. Circa la reale esistenza di questa barriera non vi è dubbio; è
stata ripetutamente confermata in laboratorio. Però è meno certo il fatto che
sia necessario, in ogni caso, uno sforzo infinito per raggiungere lo zero
assoluto. Il terzo principio è vincolante sempre e ovunque? Questo è
1’interrogativo che aleggia tra le quinte del dramma al suo inizio a
Gainesville.
Il
terzo principio puo essere violato?
Il
fatto che si possa perfino fare questa domanda risale alla natura statistica
dell’ordine. All’inizio,
vi è una probabilità piccola ma finita che un oggetto raggiunga una
temperatura di un miliardesimo di kelvin, o perfino lo zero. Per sistemi
macroscopici, come blocchi di rame, formati da trilioni di atomi, questa
probabilità è praticamente nulla. Un
atomo da solo, d’altro canto, potrebbe facilmente passare al suo stato
fondamentale e, quindi, allo stato di zero assoluto, se un concetto del genere
fosse applicabile. Ma non è cosi. La temperatura è una misura del moto casuale, 1’energia
termica, di un gruppo di particelle e perde di significato con un solo atomo.
Cosi, qualunque dubbio possa essere sollevato dal terzo principio, questo
riguarda la materia che sta tra le scale macroscopica e microscopica, in
particolare materia che si avvicina all’estremità piccola dello spettro, dove
la statistica è piu favorevole (minor numero di atomi significa minori modi di
essere disordinati). In
anni recenti, oggetti di questo tipo, detti mesoscopici per il loro stato
intermedio, hanno catturato 1’attenzione dei fisici. Contenendo
un piccolo numero di atomi e, quindi, essendo visibili soltanto con potenti
microscopi, occupano una terra di nessuno dove la resistenza elettrica, che è
normalmente una proprietà stabilita dei materiali, cambia in larga misura; dove
una perturbazione da una parte dell’oggetto può influenzare 1’altra; dove,
in breve, le leggi ordinarie della fisica non sembrano sussistere. C’è la
possibilità che gli oggetti mesoscopici abbiano la dimensione giusta per
colmare il salto tra un microkelvin e lo zero. E a questa tenue possibilità
statistica che sono appese le speranze dei fisici di Gainesville. Il loro
processo di refrigerazione, detto magnetico, è diviso in due stadi. Durante il
primo stadio, campioni di rame verranno posti tra i poli di un potente
elettromagnete e raffreddati alla più bassa temperatura raggiungibile con i
mezzi convenzionali, immergendoli in elio liquido. Nel secondo stadio, quello
decisivo, il magnete verrà spento e la temperatura del rame scenderà
spontaneamente, entro due o tre giorni, ad un valore ancora più basso. Il
raffreddamento magnetico si basa sul principio che il calore rappresenta il moto
disordinato delle particelle che costituiscono 1’oggetto. Dal momento che i
nuclei atomici si comportano come minuscoli magneti, essi rispondono a un campo
magnetico esterno, allineandosi in un’orientazione parallela, nord verso nord,
sud verso sud. Quando il campo viene eliminato, i nuclei vengono riportati in
orientazioni casuali dalle collisioni con i nuclei vicini. Tali collisioni
rallentano gli atomi, con la conseguente riduzione della temperatura. (Il
raffreddamento magnetico ricorda il raffreddamento di un elastico che viene
allungato e mantenuto per pochi secondi fino al raggiungimento della temperatura
ambiente. Quando la tensione viene allen- tata bruscamente, 1’elastico appare
notevolmente piu freddo al margine superiore). Il processo puo essere ripetuto
più e più volte, ma le difficoltà tecniche aumentano ogni volta. Un problema
particolarmente insidioso alle temperature vicine allo zero assoluto è il
contributo in quantità minima di calore dovuto alla radioattività residua nei
materiali da costruzione. ”Fallout”, tra le altre cose, da test nucleari
nell’atmosfera degli anni ’50 e, presumibilmente dal disastro di Chernobyl,
che avvenne nel 1986, ora ricopre tutta la terra. Questo rende difficile il
reperimento di metalli privi di scorie radioattive o non contaminati durante la
fabbricazione di parti di macchine quando, in forma liquida, erano esposti
all’atmosfera alla superficie dei loro contenitori. Gli scienzati di
Gainesville sperano che questo problema sia così piccolo da non produrre
effetti sui loro frigoriferi. Perfino nelle migliori condizioni, il cammino
verso lo zero assoluto non sarà né corto né facile. Da parte sperimentale, le
macchine frigorifere diventeranno sempre piu grandi, più complesse e più
costose, al diminuire delle dimensioni dei campioni. Gli accorgimenti per
1’isolamento richiederanno sforzi eroici perchè sarà sempre più difficile
accorgersi delle fughe di calore. Sul versante teorico, il terzo principio della
termodinamica deve, ad un certo panto, accordarsi con il comportamento
meccanico-quantistico dei sistemi mesoscopici. La formulazione finale deve
perdere la concisione dell’enunciato di Nernst che lo zero assoluto è
irraggingibile, ma verrà a sfiorare argomenti filosofici a proposito del
significato della meccanica quantistica (qual è il legame tra la casualità in
termodinamica e la casualità nella teoria quantistica?), della termodinamica
(quanto è a nostra conoscenza sulla raggiungibilità dello zero assoluto, come
si rifletterà sulla nostra concezione del secondo principio, che pure si basa
su una comprensione del comportamento atomico in termini statistici?) e del
procedimento di misura (come classificare un termometro che misurerà
temperature straordinariamente basse senza assorbire esso stesso calore?). La
ricerca lungo queste direttive è appena agli inizi. Il terzo principio potrebbe
finire nei libri di storia come un errore. Potrebbe venire liquidato come una
banale osservazione pratica simile all’affermazione che nessun oggetto può
avere un’energia infinita, perchè non vi è sufficiente energia disponibile
nell’universo. Potrebbe venire scoperto un nuovo fenomeno nella scala dei
microkelvin che renderebbe 1’intera discussione obsoleta. Oppure, al
contrario, 1’affermazione di Nernst, per la sua intrinseca natura
quanto-meccanica, potrebbe apparirci, di tutti i principi termodinamici, il più
significativo. Di fronte a cosi tante possibilità, viene in mente un commento
di Niels Bohr, il padre della meccanica quantistica:
L’opposto
di un’affermazione corretta è un’affermazione falsa. Ma l’opposto di una
profonda verità potrebbe ancora essere un’altra profonda verità.
Diversamente
dal primo e dal secondo principio della termodinamica, il terzo principio
risulta affascinante proprio perche potrebbe ancora far scaturire una
contrastante verità.