In questa pagina:
Problema 1: raffreddamento dell’aria umida
Problema 2: condizionatore d’aria
Richiami teorici
Compito d’esame 1: massimo lavoro estraibile da una massa d’aria
Compito d’esame 2
Compito d’esame 3: "scatolone" adiabatico
File excel per verificare le soluzioni dei compiti d'esame
Problema 1: raffreddamento dell’aria umida
Sia data, in un sistema chiuso, una massa di 10 kg di aria umida, a temperatura T1 e grado igrometrico j. Tale massa, a pressione atmosferica costante, venga poi raffreddata fino ad una temperatura T3. Si richiede il valore del calore Q da sottrarre al sistema per raggiungere la temperatura T3, e la massa di acqua che eventualmente condensa.

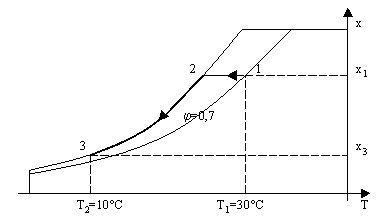
Fig.1 – Diagramma psicrometrico relativo al problema.
Dati:
Massa totale della miscela: Mtot = 10kg
Temperatura iniziale della miscela: T1 = 30°C
Grado igrometrico iniziale dell’aria: j =0,7
Pressione: P = P0 = 1bar
Calore assorbito durante il processo: Q = ?
Massa di acqua condensata durante il processo: Mcond = ?
Soluzione
Osservando lo schema del diagramma psicrometrico in figura, si può notare come la trasformazione avvenga secondo un percorso divisibile in 2 parti:
1à2: il sistema si raffredda mantenendo costante il titolo della soluzione aria – vapore d’acqua, partendo da una temperatura di 30°C, fino a quando non si arriva alla saturazione, cioè fino a quando, sul diagramma, non si raggiunge il punto 2 situato sulla curva limite;
2à3: il sistema continua a raffreddarsi fino a 10°C, proseguendo però sulla curva limite di saturazione: durante questo processo il titolo non rimane più costante, ma una quantità di vapore acqueo via via crescente condensa con l’abbassarsi della temperatura.
La prima cosa da notare è che siamo in presenza di un sistema chiuso e che tutti i fenomeni avvengono a pressione atmosferica, considerata pari ad 1 bar. Possiamo di conseguenza utilizzare il primo principio della termodinamica, di seguito riportato in forma entalpica.
![]()
Dalla invarianza della pressione si ottengono poi le seguenti due espressioni, la prima relativa all’entalpia H, la seconda all’entalpia specifica J.
![]()
![]() (1)
(1)
Il problema dunque si restringe al solo calcolo del salto d’entalpia. Dalla teoria sulle miscele di aria e vapor d’acqua (vedere apposita sezione) si riportano la formula (2) per il calcolo dell’entalpia specifica J e quella (3) per il calcolo del titolo x:
![]() (2)
(2)
![]() (3)
(3)
nella quale Ptot indica il valore della pressione globale della miscela, che per ipotesi è pari alla pressione atmosferica, cioè 1 bar, mentre la pressione parziale del vapore di saturazione PS (espressa in bar) viene ricavata dalla Tab.1
|
Temp. (°C) |
PS (mbar) |
PS (mm Hg) |
|
-15 |
1,63 |
1,24 |
|
-10 |
2,56 |
1,95 |
|
-5 |
3,96 |
3,01 |
|
0 |
6,00 |
4,58 |
|
2 |
7,05 |
5,29 |
|
4 |
8,12 |
6,10 |
|
6 |
9,345 |
7,01 |
|
8 |
10,72 |
8,05 |
|
10 |
12,77 |
9,21 |
|
12 |
14,01 |
10,05 |
|
14 |
15,96 |
12,0 |
|
16 |
18,16 |
13,6 |
|
18 |
20,62 |
15,5 |
|
20 |
23,36 |
17,5 |
|
22 |
26,42 |
19,8 |
|
24 |
29,82 |
22,4 |
|
26 |
33,60 |
25,3 |
|
28 |
37,78 |
28,4 |
|
30 |
42,41 |
31,8 |
|
32 |
47,53 |
35,3 |
|
34 |
53,18 |
39,5 |
|
36 |
59,40 |
44,2 |
|
38 |
66,24 |
49,3 |
|
40 |
73,75 |
54,9 |
|
42 |
81,98 |
61,0 |
|
44 |
91,00 |
67,8 |
|
46 |
100,86 |
75,1 |
|
48 |
111,16 |
83,2 |
|
50 |
123,35 |
92,0 |
Tab.1 – Pressione parziale del vapore di saturazione
Per prima cosa si procede al calcolo del titolo x1 (che, osservando il diagramma psicrometrico relativo all’esercizio, risulta uguale a x2) e del titolo x3, sostituendo i valori numerici nella (3). I valori di pS1, pari a 0,04241 bar e di pS2, pari a 0,01277 bar, si ricavano dalla Tab.1, che esprime la pressione parziale del vapore nella miscela in condizioni di saturazione a seconda delle varie temperature.
![]()
![]()
Per ricavare l’entalpia specifica è ora sufficiente sostituire nella (2) i valori numerici dei titoli in 1 e in 3 appena ricavati.
![]()
![]()
Per ricavare quindi la quantità di calore Q da sottrarre al sistema per ottenere la trasformazione in esame, bisogna sostituire nella (1) i valori di entalpia specifica appena ricavati. Prima di fare ciò, però, è necessario ricavare il valore MA della massa d’aria secca, che corrisponde solo ad una parte dei 10 kg di massa totale data. Partendo dalla definizione di titolo
![]()
e considerando che la massa totale della miscela è la somma delle masse di aria e di gas
![]()
si ricava facilmente il valore della massa della sola aria, sostituendo al posto del generico titolo x il valore x1 ricavato dalla prima parte della risoluzione:
![]()
Ora sono disponibili tutti i valori numerici per risolvere la (1) e ricavare il valore di Q:
![]()
Il valore ricavato di Q potrebbe apparire troppo elevato, in realtà bisogna tenere conto del fatto che parte di questa energia viene utilizzata dall’acqua come calore latente, cioè come calore di vaporizzazione.
Per calcolare in fine la massa di acqua condensata durante il raffreddamento, basta semplicemente moltiplicare il valore MA della massa d’aria secca per la differenza dei titoli:
![]()
Osservazioni
Nell’esercizio precedente si è potuto vedere come, raffreddando 10 kg di aria umida, si possa ottenere circa 1hg di acqua. Tenendo conto del fatto che 1m3 d’aria pesa circa 1,2-1,3 kg, è interessante notare quanta aria e quanto vapore d’aria siano presenti, ad esempio, in un’aula universitaria di 120m2 alta 6m: in un volume di 720m3 è presente circa una tonnellata di aria umida nella quale sono vaporizzati circa 10 litri d’acqua (è da notare che nell’esercizio di cui sopra rimane anche un titolo residuo relativo all’aria raffreddata e deumidificata).
INIZIOProblema 2: condizionatore d’aria
Il condizionatore in figura preleva aria a temperatura T1 dall’esterno attraverso la bocchetta A, grazie all’azione della ventola B alimentata esternamente. All’aria così aspirata viene sottratto del calore tramite una batteria alettata (una serie di lamierini di alluminio attraverso i quali passa l’aria), contrassegnata in figura con la lettera C. In seguito al raffreddamento, l’aria raggiunge la temperatura incognita T2, e una parte di vapore contenuto in essa condensa. L’acqua che precipita viene raccolta da una seconda serie di lamierini zigrinati (sezione D in figura), i quali hanno la funzione di far defluire il liquido attraverso il canale di scolo F. L’aria trattata, prima di essere espulsa nell’ambiente, viene postriscaldata da una seconda batteria alettata (E), al fine di evitare l’emissione di aria satura fredda.
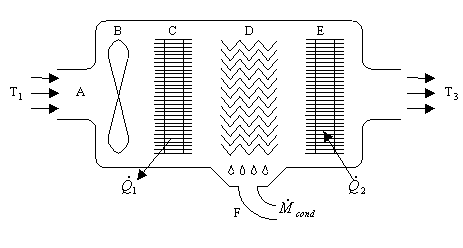
Fig.2 – Condizionatore d’aria
Il condizionatore viene montato in un’aula di 470 m3, e si richiede che l’ambiente sia sottoposto ad un ricambio orario, cioè che ogni ora venga ricambiato un volume d’aria pari al volume dell’ambiente stesso. Il tutto avviene a pressione atmosferica costante.
Dati
Pressione: P = 1 bar
Temperatura dell’aria esterna: T1 = 32°C
Grado igrometrico dell’aria esterna: j1 = 0,8
Temperatura dell’aria trattata: T3 = 20°C
Grado igrometrico dell’aria tratta: j3 = 0,5
Potenza fornita dalla ventola B: ![]()
Volume dell’ambiente: V = 470m3
Temperatura dell’aria dopo il raffreddamento: T2 = ?
Portata del tubo di scolo F: ![]()
Potenza assorbita dalla batteria C: ![]()
Potenza ceduta dalla batteria E: ![]()
Soluzione
È possibile schematizzare il processo proposto dal problema osservando il percorso sul diagramma psicrometrico
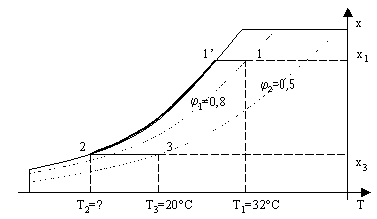
Fig.3 – Diagramma psicrometrico relativo all’esercizio
1à1’: l’aria entra ad una temperatura di 32°C e viene raffreddata a titolo costante (batteria C) fino a quando compare la prima goccia d’acqua liquida, cioè fino a quando non comincia a condensare il vapore;
1’à2: l’aria continua a raffreddarsi mentre una quantità sempre maggiore di vapore si condensa: il titolo della miscela di conseguenza si abbassa, e il percorso segue la linea di saturazione sul diagramma fino a quando viene raggiunta la temperatura incognita T2;
2à3: l’aria viene in fine postriscaldata dalla batteria E, mantenendo ovviamente il titolo costante, fino a raggiungere la temperatura T3 di 20°C.
Per prima cosa si ricavano i titoli x1 e x3 dell’aria in ingresso e in uscita dal condizionatore, tramite la (3), tenendo presente che nel punto 1 e nel punto 3 la temperatura vale rispettivamente 32°C e 20°C. Sostituendo i valori numerici si ottiene
![]()
![]()
Per ricavare il valore della massa di condensato da espellere è sufficiente moltiplicare il valore della massa d’aria secca che viene trattata per la differenza dei titoli appena ricavati. Quello che interessa, tuttavia, è la portata in massa di condensato: analogamente per ricavare questo valore la moltiplicazione da eseguire è tra la portata in massa dell’aria trattata e la differenza di titoli.
![]() (4)
(4)
I dati del problema, però, danno solo informazioni relative alla portata in volume dell’aria da trattare, non in massa. Per ricavare una portata dall’altra è necessario considerare l’aria secca come un gas perfetto ed applicare la relativa equazione di stato:
![]() (5)
(5)
Grazie a questa equazione è facilmente ricavabile la portata di aria cercata, assumendo come temperatura T il valore T3 di 20°C, poiché la portata volumetrica che il condizionatore deve sopportare è relativa all’aria che esce a 20°C, e non a quella che entra dall’esterno a 32°C. È inoltre da notare il fatto che è ancora ignota la pressione parziale dell’aria secca pA che compare in (5). Per ricavare pA basta considerare che
![]()
da cui, considerando ptot pari alla pressione atmosferica di 1 bar, e sfruttando la definizione di grado igrometrico j, si ricava
![]()
Sostituendo infine i valori numerici, la pressione parziale dell’aria secca risulta essere
![]()
(il valore di pS3 viene ricavato dalla Tab.1 per una temperatura di 20°C)
Sostituendo i valori numerici nella (5) si ottiene
![]()
Si notino alcune cose: il valore T3 è espresso in gradi kelvin, come richiede l’equazione di stato dei gas perfetti, in oltre, per ottenere una portata in chilogrammi orari, (essendo 470 il valore di metri cubi orari), il valore di pA è stato espresso in chilopascal. In fine la costante RA è stata ricavata dalla costante dei gas perfetti R0 secondo la seguente formula:
![]()
in cui mA rappresenta la massa molare dell’aria secca, considerata pari a 29kg/mol, mentre R0 è espressa in unità del S.I.
A questo punto è possibile sostituire i valori numerici nella (4)
![]()
Proseguendo, per calcolare la temperatura T2 dell’aria all’uscita dalla batteria alettata C, è opportuno notare dal diagramma psicrometrico l’uguaglianza dei titoli x2 e x3. Di conseguenza, tramite la (3) è possibile calcolare la pS2, pressione parziale del vapore di saturazione nel punto 2:
![]()
in cui il valore di j è considerato unitario dal momento che il punto 2 si trova sulla curva limite del diagramma psicrometrico. Proseguendo coi calcoli si ottiene
![]()
Osservando ora la Tab.1 si risale, da una pressione di 12mbar, a stabilire, interpolando, che la temperatura T2 dell’aria è pari a circa 9,5°C.
Passando a calcoli di tipo energetico, per ricavare le potenze assorbite e cedute rispettivamente dalle batterie alettate C ed E, è opportuno procedere con dei bilanci energetici, considerando, come convenzione, positive le entalpie uscenti dal sistema e negative quelle entranti. Più dettagliatamente, per ricavare il valore della potenza assorbita dalla prima batteria, si consideri il sottosistema formato dalla prima parte del condizionatore, cioè dall’aria che entra alla temperatura di 32°C, passa dalla batteria stessa cedendo calore, perde una certa quantità di vapore per condensazione e procede verso la seconda parte della macchina ad una temperatura di 9,5°C. Si consideri che il tutto avviene grazie all’energia fornita dalla ventola B (nel disegno il sistema equivale alle sezioni A, B, C, D ed F). Per questo sottosistema si può scrivere il seguente bilancio energetico:
![]() (6)
(6)
in cui J1 e J2 sono le entalpie specifiche dell’aria nei punti 1 e 2, cioè dell’aria che entra a 32°C (punto 1, entalpia considerata negativa) e che esce a 9,5°C (punto 2, entalpia positiva), calcolabili con le seguenti formule, sostituendo i valori noti nella (2):
![]()
![]()
L’entalpia hliq che appare nella (6) è relativa alla massa di acqua che condensa contro i lamierini zigrinati (sezione D), la quale si calcola con la seguente formula:
![]() (7)
(7)
in cui il calore specifico CL ha, come noto per l’acqua, il valore di 4,187 kJ/kg°K, mentre Tcond rappresenta la temperatura dei lamierini zigrinati. Questa temperatura, tuttavia non è uguale a quella dell’aria in questa sezione, cioè 9,5°C, poiché la batteria di lamierini, essendo bagnata (l’acqua vi condensa contro), sicuramente si troverà ad una temperatura leggermente inferiore a quella dell’aria da cui è attraversata. Approssimativamente si può considerare la temperatura Tcond pari a 8°C. Sostituendo nella (7) i valori numerici indicati, si ottiene
![]()
L’ultimo addendo da considerare prima di risolvere la (6) rispetto alla potenza assorbita dalla batteria C, è il termine![]() , che rappresenta la potenza fornita dalla ventola, e che è pari a –0,45kW (il segno meno, come da convenzione, sta ad indicare che la potenza è entrante nel sistema, cioè fornita dall’esterno). Sostituendo nella (6) i valori numerici, ed esplicitando rispetto a Q1, si ottiene
, che rappresenta la potenza fornita dalla ventola, e che è pari a –0,45kW (il segno meno, come da convenzione, sta ad indicare che la potenza è entrante nel sistema, cioè fornita dall’esterno). Sostituendo nella (6) i valori numerici, ed esplicitando rispetto a Q1, si ottiene
![]()
in cui il termine 1/3600 è stato introdotto per trasformare le portate in massa ricavate finora in chilogrammi all’ora, in portate al secondo, in modo da ottenere il risultato in chilowatt.
Passando al calcolo della potenza rilasciata dalla batteria E, il bilancio energetico che serve, analogamente a quanto appena calcolato, è appunto quello relativo alla sezione E, cioè bisogna considerare l’aria che entra ad una temperatura di 9,5°C ed esce ad una temperatura di 20°C per effetto del calore rilasciato dalla batteria:
![]() (8)
(8)
In questo caso non entrano energia dall’esterno, né si hanno perdite di massa per condensazione. L’unico termine ancora ignoto è J3, il quale viene calcolato tramite la (2), considerando una temperatura di 20°C, cioè quella dell’aria in uscita.
![]()
Sostituendo i relativi valori nella (8) si ottiene il valore cercato
![]()
Richiami teorici sulle miscele di gas e vapore
La seguente sezione vuole essere un semplice richiamo dei concetti fondamentali della teoria sulle miscele aria – vapore atto a permettere una migliore comprensione degli esercizi appena svolti. Per una trattazione approfondita si rimanda alle specifiche dispense.
Nell’aria presente in atmosfera è sempre disciolta una parte di vapore acqueo il quale, tuttavia, alla stregua dell’aria stessa, può essere considerato come gas perfetto, con massa molare pari a 18 kg/kmol, vista la composizione della sua molecola elementare (H2O). Il valore della massa molare dell’aria, invece, in base alla composizione di tale gas, è mediamente uguale a 29 kg/kmol.
In un sistema composto da una miscela aria vapore, è da sottolineare il fatto che la massa totale può non conservarsi: mentre l’aria in complesso non varia, infatti, il vapore è soggetto a variazioni, a causa di fenomeni di condensazione che possono avvenire in seguito a variazioni di temperatura o pressione causate dall’esterno. Il vapore può quindi diminuire se una parte di esso precipita in acqua e viceversa. È per questo motivo, ad esempio, che viene introdotta l’entalpia specifica J riferita alla massa d’aria secca del sistema e non, come qualsiasi grandezza specifica dovrebbe essere, riferita alla massa totale di miscela.
Per identificare la quantità di vapore presente in una determinata massa d’aria si introduce il titolo x, cioè il rapporto tra la massa di acqua evaporata e la massa d’aria secca presente (non la massa di miscela)
![]()
Il titolo della miscela può variare tra 0 (aria secca) ed il valore xS (titolo di saturazione), ma non può andare oltre: se ad una miscela a titolo xS (miscela satura) venisse aggiunto altro vapore, il vapore in eccesso (escludendo particolari situazioni metastabili) precipiterebbe sottoforma di acqua. Il valore di xS è dipendente sia dalla temperatura che dalla pressione a cui si trova la miscela. Per ricavare il valore xS nel caso specifico è necessario l’utilizzo di apposite tabelle, oppure, se la miscela si trova a pressione di 1 bar, si può utilizzare il diagramma psicrometrico, schematizzato in entrambi gli esercizi precedenti. Per ogni temperatura (in un range opportuno), corrispondente ad un punto sulle ascisse, è determinato il valore di xS, dato dall’ordinata del punto di intersezione tra la retta verticale corrispondente alla temperatura data e la curva limite riportata sul diagramma.
Oltre al titolo si definisce un’ulteriore grandezza, il grado igrometrico j, dato dal rapporto tra la pressione parziale del vapore presente in miscela e la pressione parziale che il vapore dovrebbe avere per saturare la miscela alle stesse condizioni di pressione e temperatura
![]()
Utilizzando l’equazione di stato dei gas perfetti, è semplice dedurre come il valore del titolo sia proporzionale al rapporto tra le pressioni dei due gas costituenti la soluzione.
![]()
in cui i m indicano i valori delle rispettive masse molari.
Considerando inoltre che la pressione parziale pv del vapore è esprimibile in funzione del grado igrometrico
![]()
e che la pressione parziale dell’aria pa è data dalla differenza tra la pressione totale della miscela e la pressione pv, è immediata la relazione che lega titolo e grado igrometrico:
![]()
In fine si ricorda che l’entalpia specifica J non è altro che la somma dell’entalpia hA di 1 kg di aria secca e dell’entalpia xhv degli x kg di vapore presenti in soluzione. In breve, l’entalpia hA si calcola con la seguente formula:
![]()
in cui il calore specifico a pressione costante cp ha, per l’aria, il valore di 1kJ/kg°K circa, mentre l’entalpia hv è data da
![]()
in cui r0 rappresenta il calore latente di vaporizzazione, e vale 2500kJ/kg, mentre il cp del vapore è pari a 1,9kJ/kg°K. Sommando le due entalpie si ottiene
![]()
INIZIO
Vengono di seguito riportati alcuni esercizi presentati negli esami passati a titolo di esempio
Compito d’esame 1: massimo lavoro estraibile da una massa d’aria
Determinare il massimo lavoro estraibile da una massa di 10kg d’aria che si trova alla temperatura T1 e alla pressione p, considerando l’ambiente a pressione atmosferica p0 di 1bar e temperatura T0
Dati:
Massa dell’aria: M = 10kg
Temperatura iniziale dell’aria: T1 = 400+EF °C
Pressione iniziale dell’aria: p = 10+D bar
Temperatura dell’ambiente: T0 = 20 °C
Pressione dell’ambiente: p0 = 1 bar
N.B. I numeri D,E,F rappresentano gli ultimi tre numeri della matricola dell’esaminando
Soluzione
Osservando il diagramma seguente si può notare come il percorso termodinamico del gas sia suddivisibile in due parti definite
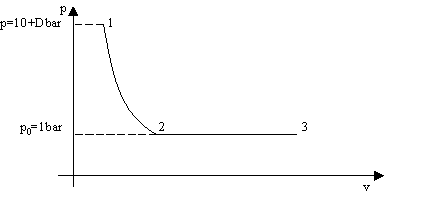
Fig.4 – Diagramma PV relativo all’esercizio
1 à 2: L’aria inizialmente compressa si espande, fino a raggiungere la pressione dell’ambiente pari ad 1bar. Si suppone che l’espansione avvenga in maniera abbastanza veloce da non permettere scambio di calore tra l’aria e l’ambiente esterno: avviene cioè un’espansione adiabatica;
2 à 3: l’aria, una volta raggiunta la pressione di 1bar, libera calore utilizzabile per produrre lavoro (ad esempio tramite una macchina di Carnot) fino a quando raggiunge la temperatura ambiente T0
Durante la prima trasformazione lo scambio di calore con l’ambiente esterno è considerato nullo, per cui il primo principio della termodinamica si riduce a
![]()
e la differenza di energia interna è facilmente calcolabile con la seguente formula:
![]()
Sembrerebbe quindi che il lavoro prodotto durante la prima parte del processo sia calcolabile tramite le due equazioni espresse. in realtà al valore così ottenuto deve essere sottratto il lavoro che viene assorbito dall’ambiente, a causa della forza esercitata dalla pressione atmosferica. Immaginando infatti l’aria racchiusa in un recipiente cilindrico, e immaginando che le sue variazioni di volume spostino uno stantuffo, si può notare come all’esterno dello stantuffo stesso non ci sia una pressione nulla, ma è presente la pressione atmosferica di 1bar. L’equazione utile per ricavare il lavoro effettivamente disponibile per gli organi meccanici di una eventuale macchina è dunque la seguente:
![]()
Per ricavare tutti i valori necessari alla soluzione della formula precedente si procede nel seguente modo: si ricava il volume iniziale dell’aria dall’equazione di stato dei gas perfetti
![]()
quindi, considerando che la pressione nel punto 2 è nota perché pari alla atmosferica, e ricordando che la trasformazione è adiabatica, si ricava il volume V2 dell’aria nel punto 2 dalla seguente identità:
![]()
In cui il valore di g per l’aria è noto e uguale circa a 1,41 (considerando l’aria come gas biatomico). Una volta ricavato V2 riutilizzando l’equazione di stato dei gas perfetti si ricava T2, e si ottengono così tutti i valori necessari al calcolo di L12.
Per quanto riguarda la seconda parte della trasformazione, è sufficiente ipotizzare che il calore rilasciato dall’aria venga utilizzato da una macchina di Carnot (la quale garantisce il massimo sfruttamento di tale calore) che lavori tra la temperatura dell’aria stessa e la temperatura ambiente. Tuttavia, man mano che si preleva calore all’aria, la temperatura della stessa non si mantiene costante, ma diminuisce progressivamente. Di conseguenza la seguente equazione, che dovrebbe essere utilizzata se la macchina lavorasse tra temperature fisse, cioè
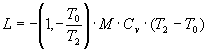
deve essere applicata in forma differenziale
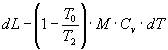
e integrata tra le due temperature estreme, cioè T2 e T0. Si ottiene così la formula risolutiva
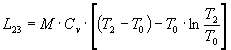
Il lavoro totale è dato dalla somma di L12 e L23.
INIZIOCompito d’esame 2
Un recipiente rigido ha un volume di 100 + EF litri. Inizialmente contiene aria secca a temperatura T1 e pressione p1. Il recipiente riceve una quantità di calore Q. A causa di questo calore l’aria raggiunge una temperatura T2 e una pressione p2. Si richiedono i valori di queste due ultime grandezze
Dati:
Volume del recipiente: V = 100+EF l
Temperatura iniziale dell’aria: T1 = 30+D °C
Pressione iniziale dell’aria: P1 = 1 bar
Calore ricevuto dal recipiente: ![]()
Temperatura finale dell’aria: T2 = ?
Pressione finale dell’aria: p2 = ?
N.B. i numeri B, C, D, E, F corrispondono al 2°, 3°, 4°, 5° e 6° numero della matricola dell’esaminando
Soluzione
Il fenomeno avviene all’interno di un recipiente chiuso ed indeformabile, di conseguenza non si ha aumento di volume e quindi non si ha produzione di lavoro. Il primo principio della termodinamica allora assume la seguente forma:
![]() (9)
(9)
La differenza di energia interna è calcolabile tramite la seguente relazione:
![]() (10)
(10)
Combinando la (9) e la (10), si ottiene la relazione
![]() (11)
(11)
in cui Q e T1 sono dati del problema, il valore del calore specifico Cv è noto, e vale approssimativamente 0,72 kJ/kg°K, mentre rimangono incognite la massa d’aria M e la sua temperatura finale T2. Per ricavare il valore della massa M si applica l’equazione di stato dei gas perfetti:
![]()
da cui
![]()
A questo punto dalla (11) posso ricavare il valore richiesto di T2, mentre l’altro valore richiesto p2 è facilmente ricavabile dall’appena utilizzata equazione di stato dei gas perfetti (la massa, il volume e la costante R sono invarianti durante il processo).
INIZIOCompito d’esame 3: "scatolone" adiabatico
Sia dato un recipiente isolato diviso inizialmente in due parti, l’una contenente ossigeno gassoso, e l’altra azoto gassoso, il primo a temperatura e pressione rispettivamente T1 e P1, mentre il secondo a temperatura e pressione T2 e P2.
L’ossigeno occupa un volume V1, mentre l’azoto occupa un volume V2. La parete che divide le due sezioni viene eliminata: si calcolino la pressione p3 e la temperatura T3 finali della miscela che si viene a formare.
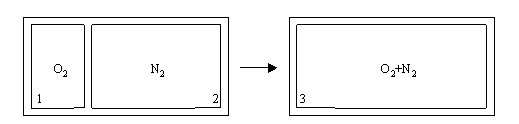
Dati:
Temperatura iniziale dell’azoto: T2 = 40+A °C
Temperatura iniziale dell’ossigeno: T1 = 5+B °C
Volume iniziale dell’azoto: V2 = 2+0,1C m3
Volume iniziale dell’ossigeno: V1 = 1+0,1D m3
Pressione iniziale dell’azoto: P2 = 2+0,1E bar
Pressione iniziale dell’ossigeno: P1 = 1+0,1F bar
Temperatura finale della miscela: T3 = ?
Pressione finale della miscela: P3 = ?
N.B. i numeri A, B, C, D, E, F corrispondono ai numeri della matricola dell’esaminando
Soluzione:
Il recipiente dentro cui avviene il processo è considerato indeformabile, per cui non vi è alcuna produzione di lavoro. In più siamo in presenza di un sistema isolato, il che significa che non avvengono scambi di calore con l’esterno. Il primo principio della termodinamica asserisce dunque che l’energia interna del sistema rimane immutata durante il processo di mescolamento dei gas. In particolare, dato che
![]()
e che l’energia interna finale corrisponde alla somma delle due energie interne iniziali associate all’ossigeno puro ed all’azoto puro, si ottiene la seguente identità:
![]() (12)
(12)
Tutti i valori che compaiono nell’equazione precedente sono noti tranne C’v, T3 e le masse M1, M2 e M3. Queste ultime le si possono ricavare dall’equazione di stato dei gas perfetti, tenendo presente che M3=M1+M2, mentre il valore medio di C’v, come noto, lo si ricava tramite la media ponderata dei Cv relativi ai singoli gas:
![]()
Sostituendo nella (12) i valori appena ricavati si calcola il valore richiesto di T3. Per trovare poi la pressione finale p3 è necessario applicare l’equazione di stato dei gas perfetti:
![]()
in cui il valore della costante R’3 si ricava come media ponderata tra le rispettive costanti R dei singoli gas:
![]()
Si ricorda in proposito che le costanti R dei singoli gas si ricavano dal rapporto tra la costante universale dei gas perfetti R0 e la massa molare dello specifico gas in esame.
Si rende disponibile un File excel per verificare le soluzioni dei compiti d'esame
INIZIO