Michele Burlenghi – matr. 1"10638– Lezione del 12/10/99 – ora 16:30-18:30
Esercizio sulle diverse metodologie di riscaldamento e relativi costi energetici.
Obiettivo.
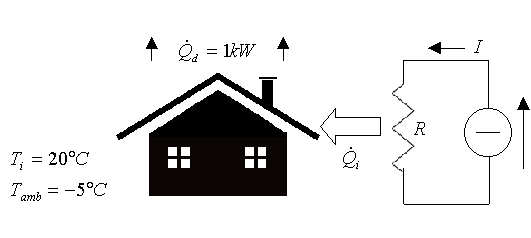
Mantenere la temperature interna (Ti) di un'abitazione ad un valore di 20 °C, quando la temperatura esterna (Tamb) è uguale a -5°C. Si supponga che, a tali temperature, il calore disperso nell'unità di tempo dall'abitazione sia pari ad 1kW.
Riscaldamento ad energia elettrica.

Figura 1 – Illustrazione del funzionamento del riscaldamento ad energia elettrica.
Utilizzando questa soluzione, il calore necessario per il riscaldamento dall'abitazione è ottenuto dalla dissipazione, per effetto Joule sulla resistenza, della potenza elettrica (L'ele) che viene fornita al sistema.
![]() (1)
(1)
Dalla (1) si deduce quindi che il coefficiente economico del sistema (e ele) è:
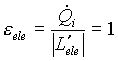 (2)
(2)
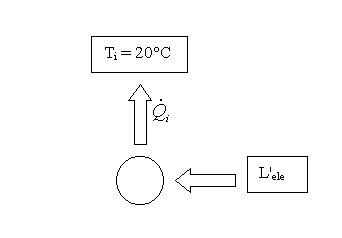
Figura 2 – Schema del funzionamento del riscaldamento ad energia elettrica.
Riscaldamento con pompa di calore elettrica.
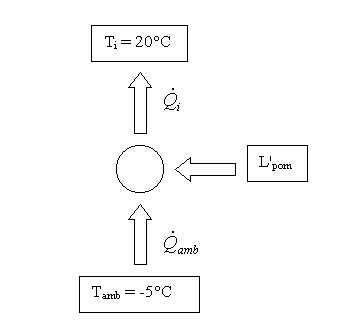
Figura 3 – Schema del funzionamento del riscaldamento con pompa di calore elettrica.
Adottando questa scelta progettuale si ottengono i seguenti risultati:
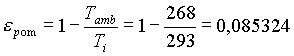 (3)
(3)
![]() (4)
(4)
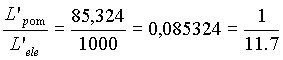 (5)
(5)
E' evidente che utilizzando la pompa di calore si ha che la potenza elettrica si riduce di molto rispetto al caso precedente, è dunque da preferirsi rispetto alla resistenza elettrica; comunque sia, questa potenza elettrica deve essere fornita da qualcuno o qualcosa, ciò implica ulteriori costi energetici.
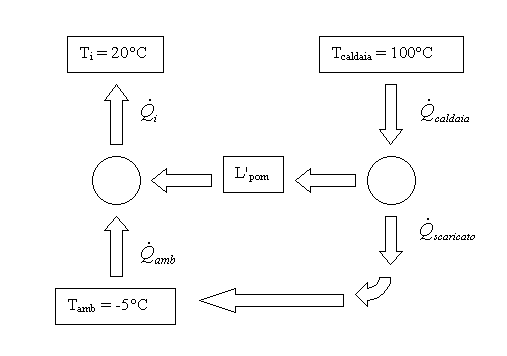
Figura 4 – Schema pompa di calore elettrica + macchina termica ciclica.
Ipotizzando che il lavoro elettrico nell'unità di tempo sia fornito da una macchina termica ciclica funzionante alle temperature Tcaldaia =100°C e Tamb=-5°C, il sistema si modifica come illustrato in Fig.4 e si procede nuovamente al calcolo dell'efficienza complessiva del sistema.
Innanzi tutto si procede al calcolo del coefficiente economico della macchina termica ciclica, che è in prima approssimazione uguale a quello di una macchina ciclica di Carnot funzionante alle stesse temperature.
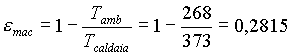 (6)
(6)
Noto e mac si può calcolare la quantità di calore che si deve estrarre del serbatoio caldo nell'unità di tempo.
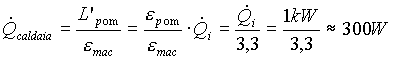 (7)
(7)
Nelle applicazioni pratiche si ha invece per la macchina termica ciclica, un coefficiente economico minore della macchina di Carnot. Si noti comunque che, nonostante sia stato introdotto nel bilancio energetico il contributo della macchina termica ciclica, questo sistema è ancora più efficiente del sistema basato sulla sola resistenza elettrica, in cui non erano inseriti i costi energetici per la produzione della potenza elettrica.
Tutti questi risultati si possono condensare nell'introduzione di due nuovi coefficienti:
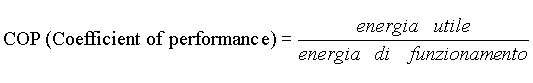

Per la pompa di calore si hanno i seguenti valori:
![]() (8)
(8)
![]() (9)
(9)
Da notare il fatto che il comportamento non ideale della macchina termica ciclica abbassa di molto il CUC del sistema.
Il teleriscaldamento di Brescia.
Il sistema di teleriscaldamento di Brescia, rappresenta l'ulteriore miglioramento sotto il profilo del rendimento energetico del sistema illustrato in Fig.4. Concettualmente l'idea su cui è basato è simile a quanto già descritto precedentemente. Le differenze sono essenzialmente due:
In questo modo si riesce a sfruttare al massimo il calore erogato dalla caldaia della centrale. Infatti, per essa si può tranquillamente stimare un coefficiente economico e centrale» 0,5, che unito al fatto dell'utilizzazione delle acque di "scarto" per il riscaldamento e all'utilizzazione delle pompe di calore può portare ad un CUC pari a:
![]() (10)
(10)
Quando il valore massimo teorico è uguale a due.
Sistemi chimicamente omogenei.
Generalità
In questa sezione vengono prese in considerazione le sostanze pure, nei loro diversi stati d'aggregazione solido, liquido ed aeriforme, Nella fase aeriforme, si usa distinguere tra vapori e gas, ma è bene rilevare subito che tale distinzione non ha riscontro nel comportamento termodinamico delle sostanze. Infatti, come si vedrà, si parla di gas o vapori a seconda che ci si trovi al di sopra (gas) od al di sotto (vapori) della temperatura di un particolare stato termodinamico, denominato punto critico.
Come base di partenza per illustrare i passaggi delle sostanze da una fase d'aggregazione all'altra, sono presi in esame i diagrammi tridimensionali (p, v, T). Dalle proiezione di tali diagrammi sui piani Cartesiani vengono ottenuti i diagrammi bidimensionali (p, T) e (p, v), più facili da rappresentare e di grande importanza concettuale.
Per la descrizione degli aeriformi quando sono verificate opportune condizioni, pressioni relativamente basse e temperature relativamente alte, si può utilizzare il modello del gas ideale, anche se non può essere utilizzato per tutte le situazioni d'interesse tecnico. E' noto, infatti, che il comportamento degli aeriformi, o gas reali, devia tanto più da quello dei gas ideali quanto più aumenta la pressione e diminuisce la temperatura. Quindi, per pressioni relativamente elevate e temperature relativamente basse, le forza d'attrazione intermolecolari ed il volume proprio delle molecole non possono più essere trascurati. Come conseguenza, l'equazione di stato dei gas ideali non è più valida, e devono essere cercate nuove relazioni funzionati tra pressione, volume specifico e temperatura assoluta.
Da un punto di vista pratico, solo le zone dei diagrammi caratterizzate dalla presenza degli stati d'aggregazione liquido ed aeriforme sono rilevanti ai fini della rappresentazione dei cicli termodinamici. Inoltre, nell'analisi dei cicli, risulta vantaggioso poter leggere sugli assi coordinati proprietà come l'entalpia e l'entropia e, in base a questi criteri, nel seguito verranno illustrare le zone comunemente utilizzate dei diagrammi (T, s), (h, s) e (p, h), tale parte è stata aggiunta per completezza, a lezione non è stata trattata.
Per il calcolo delle proprietà delle sostanze chimicamente pure, vedere la prossima lezione.
Diagrammi (p, v, T) e (p, T)
Nel caso di un fluido che cambia stato d'aggregazione, la relazione tra pressione, volume specifico e temperatura può essere rappresentata mediante diagrammi tridimensionali come quelli riportati in Fig.5. Tali diagrammi vengono chiamati
(p, v, T) dal nome delle coordinate Cartesiane scelte per la rappresentazione o, in alternativa, vengono detti "collinari" per il loro aspetto. In base alla più volte richiamata regola delle fasi, quando un'unica sostanza (M = 1) è presente con una sola fase (F = 1), gli stati del sistema risultano determinati dalla specificazione di due sole proprietà intensive (P = M + 2 - F = 2). Pertanto, in presenza di un'unica fase, gli stati del sistema appartengono ad una superficie f(p,v,T)=0 che prende il nome dalla fase stessa: solido S, liquido L, vapore V e GAS. Nelle zone di coesistenza tra le diverse fasi: (S-V), (S-L) ed (L-V), si ha invece F = 2 e, di conseguenza, gli stati del sistema risultano determinati dalla specificazione di una sola proprietà intensiva (P = M + 2 - F = 1).
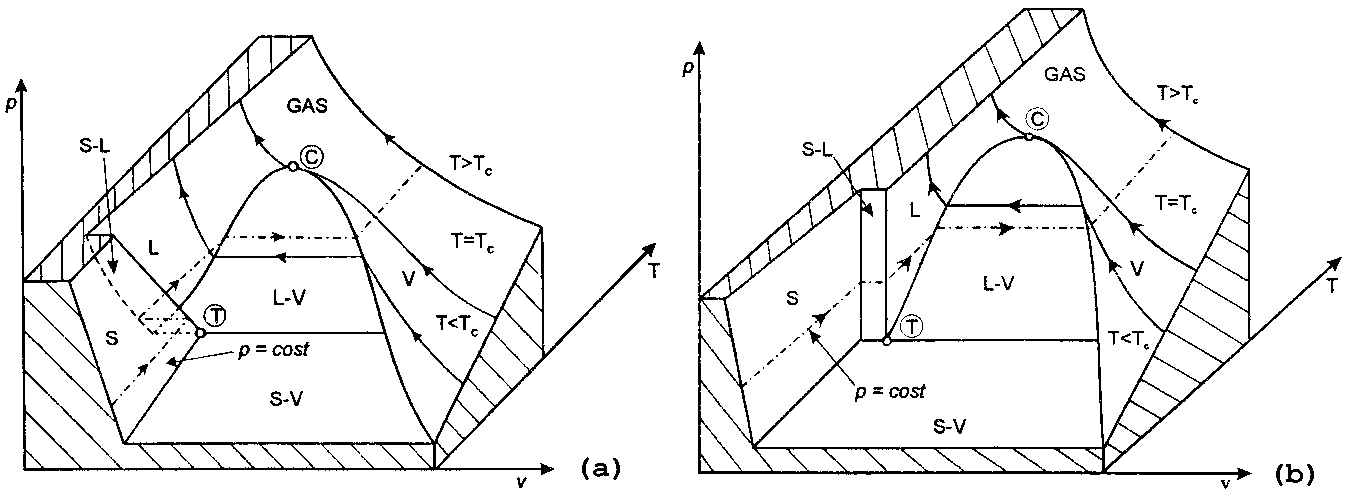
Figura 5 – Diagramma collinare per sostanza, come l'acqua, che diminuisce di volume durante la fusione (a) o che aumenta di volume durante la fusione (b).
In questo caso, gli stati del sistema appartengono a superfici d'equilibrio sulle quali, ad esempio, pressione e temperatura non possono variare indipendente una dall'altra. Infine, la presenza contemporanea di tre fasi (S-L-V) individua la linea del punto triplo, in corrispondenza alla quale si ha F = 3 e P = 0. Nella linea del punto triplo "T", il sistema non ha gradi di libertà e, infatti, sia la pressione sia la temperatura risultano indipendenti dalle frazioni di solido, liquido e vapore presenti.
Per tutte le sostanze, il passaggio da liquido a vapore avviene a temperature tanto più elevate quanto maggiori sono le pressioni, e sempre con aumenti di volume specifico. Invece, durante la fusione il volume specifico può diminuire, come nel caso dell'acqua, od aumentare, come nella maggior parte delle sostanze. Le sostanze come 1'acqua, che diminuiscono di volume durante la fusione, danno luogo ad un diagramma del tipo rappresentato in Fig.5 (a), dove la fusione avviene a temperature tanto più basse quanto maggiori sono le pressioni. La maggior parte delle sostanze, dà luogo invece ad un diagramma del tipo rappresentato in Fig.5 (b), dove la fusione avviene a temperature tanto più alte quanto maggiori sono le pressioni.
Nella Fig. 5, sono illustrati gli andamenti di un'isobara e di tre isoterme, L'isobara evidenzia il comportamento del volume specifico e delle temperature durante i cambiamenti di fase, mentre le isoterme evidenziano la possibilità, o meno, di entrare nella zona d'equilibrio liquido-vapore aumentando la pressione. Se la temperatura è minore di quella del punto critico "C", aumentando la pressione si porta la sostanza prima allo stato d'equilibrio liquido-vapore e, successivamente, allo stato liquido. Se invece la temperatura è superiore a quella critica la sostanza non può essere portata allo stato d'equilibrio liquido-vapore per quanto venga aumentata la pressione. In base a questa distinzione, se la temperatura è minore di quella critica si preferisce parlare di vapore, mentre se la temperatura è superiore di quella critica si preferisce parlare di gas. Va, tuttavia, precisato che vapori e gas non sono altro che aeriformi e quindi non differiscono per lo stato d'aggregazione: la distinzione tra essi è convenzionale ed è basata unicamente sulla temperatura (minore o maggiore della temperatura critica alla quale l'aeriforme si presenta.
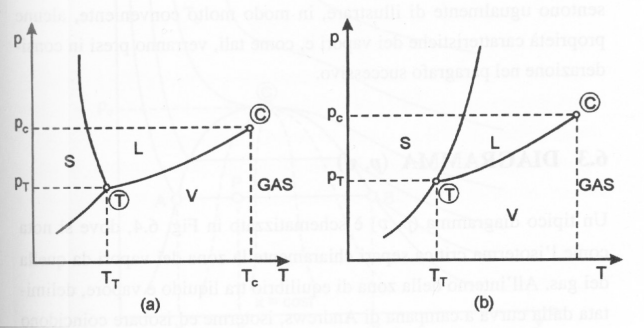
Figura 6 – Diagramma (p, T) per fluidi che si comportano come l'acqua (a) o come la maggior parte delle sostanze (b).
Le diverse fasi. e le zone di coesistenza tra le fasi, sono ben individuate nei diagrammi (p, T), ottenuti proiettando il diagramma collinare sul piano pressione-temperatura. Attraverso questa proiezione si arriva a diagrammi del tipo di quelli rappresentati in Fig.6, dove sono evidenziati i comportamenti di fluidi come l'acqua, in Fig, 6 (a), o come la maggior parte delle sostanze, in Fig.6 (b). Il particolare andamento della curva d'equilibrio solido-liquido in Fig.6 (a) giustifica il fatto che il punto di fusione del ghiaccio a pressione atmosferica (101,325 kPa) si trovi a temperatura inferiore a quella del punto triplo dell'acqua (PT = 0,61 kPa <patm).
Invece, per la maggior parte delle sostanze, il diagramma di Fig. 6 (b) indica che l'equilibrio solido-Iiquido si sposta verso temperature più alte a pressioni superiori a quella punto triplo.
Tabella 1 – Punto triplo e punto critico d'alcune sostanze.
|
Sostanza |
PT [kPa] |
TT [K] |
PC [kPa] |
TC [K] |
|
CH4 |
11,72 |
90,68 |
4595 |
190,56 |
|
CO2 |
517 |
216,48 |
7377 |
304,20 |
|
H20 |
0,61 |
273,16 |
22055 |
647,13 |
|
N2 |
12,53 |
63,50 |
3390 |
126,20 |
|
NH3 |
6,10 |
195,49 |
11304 |
405,36 |
|
O2 |
0,15 |
54,36 |
5043 |
154,58 |
|
R134a |
0,39 |
169,85 |
4056 |
374,18 |
A conclusione del paragrafo, si può osservare che i diagrammi tridimensionali possono venir rappresentati in piano solo approssimativamente, mentre i diagrammi bidimensionali (p, T) non consentono di riportare le variazioni dei potenziali termodinamici durante i cambiamenti di stato. Per superare queste limitazioni sarebbe possibile utilizzare, in linea di principio, i diagrammi (p, v), ottenuti proiettando i diagrammi collinari sul piano pressione-volume specifico. Tuttavia, i diagrammi (p, v) dei vapori non si prestano molto agli usi tecnici, dal momento che non vengono quasi mai disegnati in scala lineare a causa delle grandi variazioni tra i volumi specifici delle fasi liquido e vapore (per l'acqua: da 0,001 a 102 m3/kg). Se la scala non è lineare, l'utilità pratica delle rappresentazioni è limitata, in quanto si perde la proporzionalità tra le aree e lavori scambiati con l'esterno. Tuttavia. i diagrammi (p, v) consentono ugualmente di illustrare, in modo molto conveniente, alcune proprietà caratteristiche dei vapori e, come tali, verranno presi in considerazione nel paragrafo successivo.
Diagramma (p, v)
Un tipico diagramma (p, v) è schematizzato in Fig. 7, dove si nota come l'isoterma critica separi chiaramente la zona dei vapori da quella dei gas. All'interno della zona d'equilibrio tra liquido e vapore, delimitata dalla curva a campana d'Andrews, isoterme ed isobare coincidono ed i cambiamenti di stato tra liquido e vapore avvengono gradualmente.
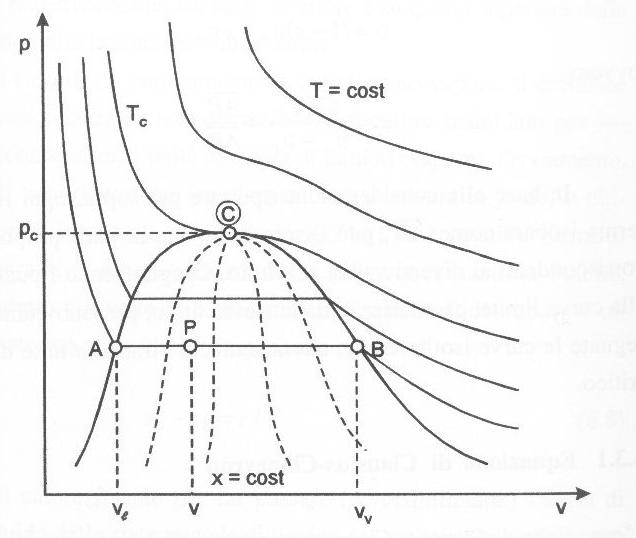
Figura 7 – Diagramma (p, v) dei vapori.
Se il fluido è composto da una miscela di liquido e vapore, il suo titolo x può essere definito conte il rapporto fra la massa del vapore e la massa totale della miscela di liquido e vapore
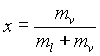 . (11)
. (11)
Pertanto, quando il titolo è uguale a zero, il punto si trova sul ramo inferiore della curva limite e lo stato corrispondente viene definito "liquido saturo". Quando invece il titolo è uguale ad uno, il punto si trova sui ramo superiore della curva limite e lo stato corrispondente viene definito "vapore saturo secco". Nella zona d'equilibrio liquido-vapore si parla, genericamente, di "vapore saturo" e, nell'ipotesi di scala lineare dei volumi, il titolo può essere determinato come in Fig. 7, trovando il rapporto tra le lunghezze dei segmenti evidenziati
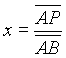 . (12)
. (12)
Infatti, tutte le proprietà estensive, dei vapori saturi possono venire espresse come somma delle proprietà dei componenti: liquido saturo, vapore saturo secco. Di conseguenza anche il volume totale occupato dalla miscela, proprietà estensiva, può venir espresso dalla relazione
![]() (13)
(13)
pertanto, con riferimento all'unità di massa di miscela, dividendo i due membri per (ml+mv) si trova
![]() (14)
(14)
ovvero
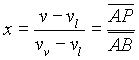 . (15)
. (15)
Indicando con
![]() (16)
(16)
il volume differenziale della miscela, dalla (14) e (16) si può esprimere v in e in funzione del titolo x
![]() . (17)
. (17)
Analogamente al volume della miscela, nella zona dei vapori saturi, si possono esprimere le altre proprietà estensive come segue
![]() (18)
(18)
![]() (19)
(19)
![]() (20)
(20)
dove ud, hd, sd, indicano rispettivamente l'energia interna, l'entalpia, l'entropia differenziali della miscela.
In base alle considerazioni riportate più sopra, ogni linea isoterma-isobara come AB, può essere suddivisa in parti proporzionali, corrispondenti ai diversi valori del titolo. Congiungendo i punti interni alla curva limite, caratterizzati dallo stesso titolo, possono quindi essere segnate le curve isotitolo che, ovviamente, si diramano tutte dal punto critico.
Liquido sottoraffreddato e vapore surriscaldato
Nella pratica, capita spesso che i termini "liquido sottoraffreddato" e Il "vapore surriscaldato" vengano usati in modo non appropriato. E' utile quindi fornire le definizioni corrette, riferite alle situazioni schematizzate nella Fig. 8.
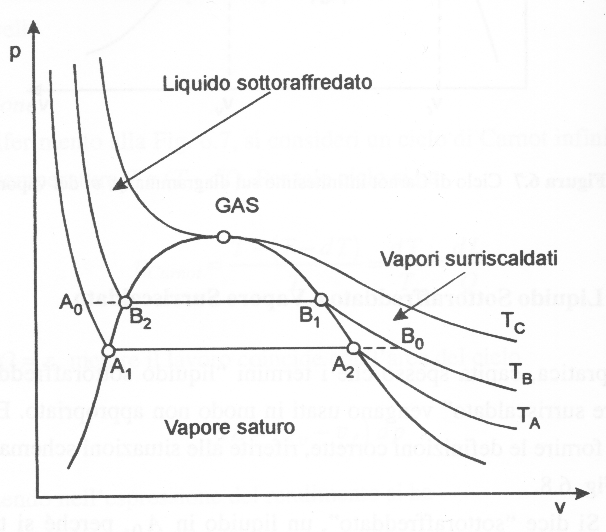
Figura 8 – Zone del liquido sottoraffreddato, del vapore saturo e surriscaldato e del gas.
Si dice "sottoraffreddato", un liquido in A0, perché si trova a temperatura TA , inferiore alla temperatura TB del liquido saturo in B2 che ha la stessa pressione, ovvero si trova a pressione pA0 superiore alla pressione pA1 del liquido saturo che ha la stessa temperatura. Pertanto, l'aggettivo sottoraffreddato non fa alcun riferimento al valore assoluto della temperatura e, di conseguenza, possono trovarsi nello stato di "sottoraffreddamento" anche liquidi a temperatura notevolmente superiore a quell'ambiente. Significativo, a questo proposito, è il caso degli impianti di riscaldamento ad acqua "sottoraffreddata", nei quali s'impiegano pressioni dell'ordine di 0,7 - 1 MPa per utilizzare acqua allo stato liquido a temperature dell'ordine di 150 - 160 °C. Naturalmente. nella pratica commerciale, il termine sottoraffreddato non appare particolarmente felice e quindi, spesso, si parla d'impianti ad acqua surriscaldata (che non esiste nello stato d'equilibrio). Più accurata ed ugualmente rispettosa delle esigenze commerciali appare, semmai, la definizione equivalente d'impianti ad acqua "pressurizzata".
Si dice invece "surriscaldato". un vapore in B0, perché si trova a temperatura TB maggiore della temperatura TA, del liquido saturo in A2 che ha la stessa pressione, ovvero si trova a pressione pB0, inferiore alla pressione pB1, del liquido saturo che ha la stessa temperatura. Pertanto, anche in questo caso, l'aggettivo surriscaldato non fa alcun riferimento al valore assoluto della temperatura e, di conseguenza, possono trovarsi nello stato di "surriscaldamento" anche vapori a temperatura ambiente. Significativo, a questo proposito, è il caso del vapor d'acqua contenuto nell'aria che risulta quasi sempre surriscaldato.
Diagramma (T, s). (non mostrato a lezione)
Il diagramma (T, s) dei vapori è schematizzato in Fig.9 dove si fa riferimento all'acqua fissando l'origine nel punto a temperatura T0 = 276,15 K (=0,01 °C) sulla curva limite inferiore.
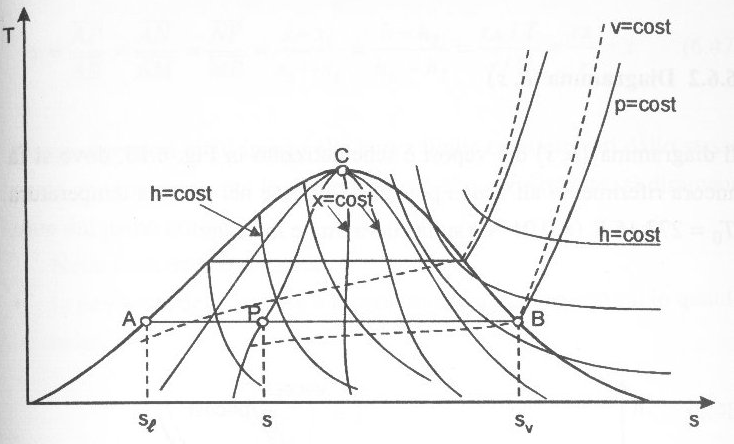
Figura 9 – Diagramma (T, s) riferito all'acqua, con origine nel punto a temperatura T0 = 276,15 K (=0,01 °C) sulla curva limite inferiore.
Nella zona del liquido sottoraffreddato, le isobare sono molto vicine alla curva limite inferiore, tanto che vengono rappresentate distinte da essa soltanto a scopi didattici, il titolo in un punto generico all'interno della curva d'equilibrio può essere determinato come in figura, trovando il rapporto tra le lunghezze dei segmenti
x =AP/AB .
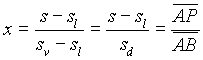 (21)
(21)
Di conseguenza, ogni linea isoterma-isobara come AB può essere suddivisa in parti corrispondenti ai diversi valori del titolo. Congiungendo i punti interni alla curva limite, caratterizzati dallo stesso titolo, vengono ottenute le curve isotitolo che, ovviamente, si diramano tutte dal punto critico.
Nel passaggio dall'interno all'esterno della zona del vapore saturo umido
mentre, nella zona degli aeriformi
Diagramma (h, s). (non mostrato a lezione)
Il diagramma (h, s) dei vapori schematizzato in Fig.10 dove si fa ancora riferimento all'acqua ponendo l'origine nel punto a temperatura T0 = 273,16 K
(= 0,01 °C) sulla curva limite inferiore.
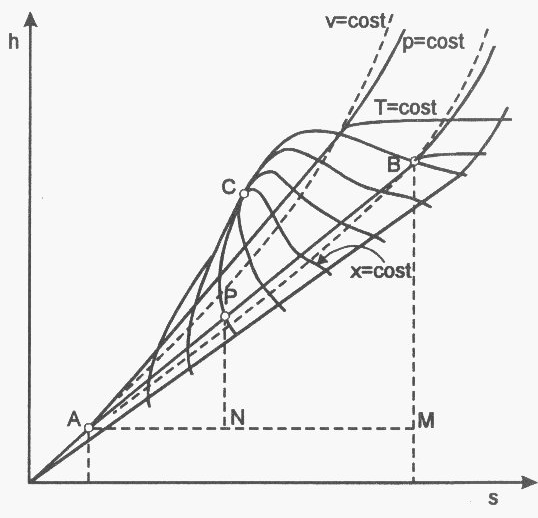
Figura 10 – Diagramma (h, s) riferito all'acqua, con origine nel punto a temperatura T0 = 276,15 K (=0,01 °C) sulla curva limite inferiore.
Il titolo in un punto generico all'interno della curva d'equilibrio può essere determinato come in figura, trovando il rapporto tra le lunghezze dei segmenti
x =AP/AB .
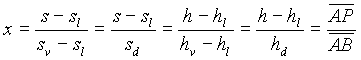 (22)
(22)
Congiungendo i punti interni alla curva limite, caratterizzati dallo stesso titolo, vengono ottenute le curve isotitolo che, ovviamente, si diramano tutte dal punto critico.
Nella zona dei vapori saturi
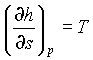 (23)
(23)
mentre essendo la temperatura una funzione continua
Nella zona dei vapori surriscaldati e dei gas
Diagramma (p, h). (non mostrato a lezione)
Il diagramma (p, h) dei vapori è schematizzare in Fig.11, dove viene impiegata una scala logaritmica per la pressione e viene fatto riferimento al fluido RI34a, utilizzato nella refrigerazione, Si osservi come, nella zona del liquido, le isoterme abbiano un andamento verticale, in quanto praticamente coincidenti con le isoentalpiche. Nella zona dei vapori, il titolo in un punto generico può essere determinato come in figura, trovando il rapporto tra le lunghezze dei segmenti evidenziati.
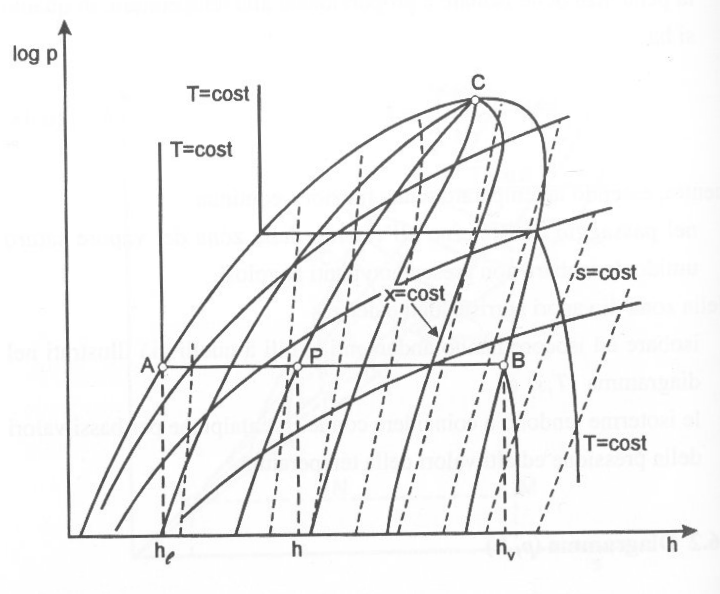
Figura 11 – Diagramma (p, s) riferito al fluido R134a, con scala logaritmica delle pressioni.
Ancora una volta, congiungendo i punti interni alla curva limite caratterizzati dallo stesso titolo, vengono ottenute le curve isotitolo che, ovviamente, si diramano tutte dal punto critico.
In tutto il diagramma
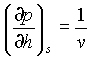 (24)
(24)
Nella zona dei vapori surriscaldati e dei gas